Novinky z PragueONCO 2022

V rámci 13. kongresu PragueONCO v Praze ve dnech 26.–28. 1. 2022 zazněly nejnovější informace z nedávných mezinárodních odborných setkání ASCO 2021, ESMO 2021 a ASCO GI 2022. Týkaly se např. novinek v léčně karcinomu slinivky břišní a podjaterní krajiny, karcinomu jícnu a žaludku, hepatocelulárního karcinomu nebo kolorektálního karcinomu.
S aktuálními poznatky z oblasti karcinomu pankreatu a podjaterní krajiny vystoupil prof. MUDr. Luboš Petruželka, CSc., Onkologická klinika 1. LF UK, VFN a ÚVN, Praha. Jak uvedl, u karcinomu slinivky břišní je ve všech jeho klinických stadiích ve srovnání s ostatními typy zhoubných nádorů doba přežití nemocných nejkratší, což platí jak pro karcinom pankreatu, tak i pro biliární karcinomy. „Pokud nemoc není léčena, u karcinomu pankreatu v pokročilých stadiích je medián přežití tři měsíce, a snaha o zlepšení je tedy nutná,“ připomněl prof. Petruželka, podle něhož k nejdůležitějším posunům v této oblasti patří aplikovaná genomická medicína. U karcinomu pankreatu byly popsány mutace u více než 600 genů a frekvence výskytu mutací nad jedno procento je asi u 40 genů, z čehož vyplývá, že část aberací je terapeuticky ovlivnitelná. Podle genomické analýzy je v současnosti možno až u 25 procent nádorů slinivky břišní odhalit řídící „targetabilní“ aberace.
Mezi zásadní nové klinické studie patří KRYSTAL‑1, která hodnotila aktivitu adagrasibu (MRTX849), což je inhibitor použitelný při mutaci KRASG12C. Mechanismus účinku nového inhibitoru v tomto případě probíhá cestou ovlivnění příslušných tyrosinkináz. Ve studii byla prezentována pacientská kohorta fáze II, která hodnotila adagrasib 600 mg 2× denně u předléčených nemocných s tím, že ve studii byla skupina pacientů s karcinomem pankreatu s přítomností této mutace. Přestože studie zkoumala poměrně malý počet nemocných s mutací KRASG12C, ukazuje se, že je to jedna z možných cest úspěšné léčby. Bude ale potřeba dalších klinických hodnocení, která tuto účinnost prověří.
K vývoji dochází i v oblasti nádorů biliárních cest, nádorů podjaterní krajiny. V současné době již FDA schválila cílenou léčbu přípravkem pemigatinib, schválen je i přípravek infigratinib a ivosidenib na základě identifikace terčových mutací.
Randomizovaná, dvojitě zaslepená a placebem kontrolovaná studie fáze III TOPAZ‑1 hodnotila inhibitor PD‑L1 durvalumab v kombinaci s gemcitabinem a cisplatinou u 685 pacientů s pokročilým nádorem biliárního traktu. V kontrolním rameni studie byla standardní léčba GemCis, experimentální rameno přidávalo pacientům durvalumab 1 500 mg. Primárním cílem studie bylo celkové přežití pacientů (OS), který ve studii byl splněn: 24měsíční přežití činilo kolem 25 procent v aktivním léčebném rameni studie. Kombinace durvalumabu s GemCis by se tedy mohla v blízké době stát standardem léčby pokročilých biliárních karcinomů.
„Praktická doporučení pro léčbu karcinomu pankreatu plynoucí z nových poznatků je provedení testování potenciálně targetabilních somatických aberací pomocí NGS DNA a RNA. Zde je problém s dostatečným množstvím bioptického materiálu. U mikrosatelitové nestability u všech nádorů s lokálně pokročilým nebo s metastazujícím karcinomem pankreatobiliárního traktu by měla být provedena vyšetření. Molekulární testování je nutné provést co nejdříve. Ukazuje se, že testování zárodečných mutací je doporučeno u všech pacientů s diagnózou karcinomu pankreatu ve všech klinických stadiích,“ shrnul prof. Petruželka.
Karcinom jícnu a žaludku
S nejnovějšími poznatky z kongresu z oblasti karcinomu jícnu a žaludku přispěla MUDr. Radka Obermannová, Ph.D., z MOÚ Brno. Přednáška byla zaměřena především na novinky v imunoterapii a v chemoterapii. Jak uvedla, výskyt nádorů jícnu a žaludku má v západní populaci sice klesající tendenci, nicméně pětileté přežití u nádorů jícnu dosahuje pouze 20 procent a u nádorů žaludku je 32procentní.
V případě adenokarcinomu jsou k dispozici dva léčebné postupy: perioperační chemoterapie anebo neoadjuvantní chemoradioterapie. Doposud však nebylo k dispozici srovnání těchto dvou léčebných přístupů. To nyní přináší nová mezinárodní studie fáze III Neo‑AEGIS. Ta randomizovala 377 pacientů s adenokarcinomem v první větvi k léčbě neoadjuvantní chemoradioterapií v rámci režimu CROSS (karboplatina AUC2 + paklitaxel 50 mg/m2) s radioterapií 41,4 Gy. Tento léčebný přístup byl srovnán ve druhé větvi s předoperační chemoterapií ECF/X nebo FLOT. Poté následovala resekce a sledování. Výsledky studie při sledování 24,5 měsíce ukázaly, že pravděpodobnost tříletého celkového přežití byla v obou ramenech stejná, což byl důvod k předčasnému ukončení studie. „Oba uvedené léčebné režimy jsou tedy použitelné a z pohledu celkového přežití rovnocenné,“ uzavřela výsledky studie MUDr. Obermannová.
Algoritmus léčby lokálně pokročilého karcinomu jícnu je v současné době obohacen o adjuvantní inhibitor PD‑1 nivolumab, který zatím v ČR není k dispozici. Běžnou praxí je dnes princip neoadjuvantní chemoterapie režimem CROSS a následná resekce. Otázkou je, jaký zvolit další postup, pokud nedojde ke kompletní remisi onemocnění a nedojde ke kompletní eradikaci nádorových buněk, a jak intenzifikovat pooperační léčbu. Pokud je pacient léčen předoperační chemoterapií, je použit režim FLOT. Nicméně 50 procent pacientů není schopno předoperační léčbu podstoupit.
Na potenciál imunoterapie v této indikaci se zaměřila studie CHECKMATE‑577, která randomizovala 794 pacientů v poměru 2 : 1 k léčbě nivolumabem nebo k placebu. Pacienti ve studii měli diagnózu adenokarcinomu nebo skvamózního karcinomu. „Primárním cílovým ukazatelem studie byl parametr disease‑free survival (DFS), který dosáhl 22 měsíců v léčebné skupině vs. 11 měsíců v placebové skupině, což je pro klinickou praxi poměrně významné,“ poznamenala MUDr. Obermannová. V analýze podskupin podle histologických typů je patrné, že oba histologické typy mají užitek z této léčby, i když výraznějšího efektu bylo dosaženo u skvamózního karcinomu. Co se týká lokalizace, menšího benefitu dosáhli pacienti, kteří měli tumor v oblasti gastroezofageální junkce. Výsledky této studie změnily guidelines ESMO i postupy v Modré knize a obohatily je právě o zařazení nivolumabu do léčebných schémat, kdy se tímto přípravkem budou léčit pacienti po operaci po dobu jednoho roku.
Další prezentovaná studie fáze III KEYNOTE‑590 se týkala stadia IV karcinomu jícnu a jeho obou histologických typů. Tato studie randomizovala pacienty k léčbě imunoterapií pembrolizumabem 200 mg + standardní chemoterapií vs. chemoterapie samotná. Primárním sledovaným cílem studie bylo celkové přežití. Pro celkové přežití u podskupiny pacientů se skvamózním karcinomem dosáhla hodnota HR = 0,57 s CPS >10, ale i v celkové skupině pacientů byl významný zisk ze sledované terapie (HR = 0,62 pro CPS > 10). Výsledky uvedené studie vedly EMA ke schválení pembrolizumabu pro léčbu metastatického onemocnění, která je velice efektivní. V ČR zatím není stanovena úhrada.
K dalším novým studiím patří i CHECKMATE‑648 zaměřená na skvamózní dlaždicobuněčný karcinom, kde bylo sledováno 970 pacientů. Studie měla tři ramena a porovnávala standardní chemoterapeutický režim vs. rameno chemoterapie + nivolumab vs. rameno nivolumab + ipilimumab. Primárním cílem studie bylo OS a studie bude kompletně prezentována v odborném tisku v květnu 2022. Nicméně již dnes lze říci, že primární cíl studie byl splněn pro pacienty s expresí PD‑1 nad 1 procento pro obě ramena, ve kterých byl použit nivolumab. „Výsledky této studie jistě budou měnit naší klinickou praxi,“ poznamenala MUDr. Obermannová.
Studie CHECKMATE‑649 prezentovaná na ESMO 2021 s follow‑up 24 měsíců byla zaměřena na karcinom žaludku. Design studie je velmi podobný designu CHECKMATE‑648 s rozdílem, že zde byli sledováni pouze pacienti s adenokarcinomem. Rameno nivolumab + ipilimumab bylo předčasně ukončeno pro výskyt nežádoucích účinků. Primárním cílem studie bylo OS a doba bez progrese onemocnění (PFS). Studie primární cíl splnila. Pacienti, kteří měli nádor větší než CPS > 5, měli medián celkového přežití 14 měsíců (nivo + chemo) vs. 11 měsíců (chemo). 24měsíční follow‑up ukázal, že efekt sledované léčby je dlouhodobý a zůstává zachován.
Další nová studie GERCOR fáze II s adenokarcinomem žaludku sleduje perioperační imunoterapii a poskytuje poměrně převratné výsledky. Primárním cílem studie bylo dosažení patologických kompletních remisí. Léčba byla nastavena na kombinaci nivolumab + ipilimumab bez chemoterapie předoperačně. Patologické kompletní remise dosáhlo téměř 60 procent pacientů, přičemž tato léčba nezpůsobila vyšší počet perioperačních komplikací.
Jak MUDr. Obermannová uzavřela, pro lokálně pokročilý karcinom jícnu a žaludku byl tento rok poměrně převratný z hlediska přínosu klinických studií. Standardem léčby lokálně pokročilého adenokarcinomu jícnu je perioperační chemoterapie nebo předoperační chemoradioterapie. Standardem léčby lokálně pokročilého adenokarcinomu žaludku je perioperační chemoterapie.
Hepatocelulární karcinom
Novinkám z oblasti hepatocelulárního karcinomu (HCC) věnoval své vystoupení MUDr. Eugen Kubala z FTN Praha. Rozvoj léčby tohoto druhu nádorového onemocnění zaznamenal od r. 2007 velký rozmach. Představeny byly studie jak pro první, tak i pro druhou linii léčby HCC.
Randomizovaná, multicentrická,
otevřená studie fáze II HIMALAYA (n = 1 324) využila velmi specifický a inovativní způsob dávkování, kde režim STRIDE, skládající se z jedné dávky 300 mg tremelimumabu (anti‑CTLA‑4) + 1 500 mg durvalumabu (anti‑PD‑L1) + 1 500 mg durvalumabu každé čtyři týdny vedl ke slibné protinádorové aktivitě a minimální toxicitě. Primárním cílem studie bylo OS pro durvalumab/tremelimumab vs. sorafenib, který byl komparátorem. Studie měla celkem čtyři ramena, kdy čtvrté rameno se standardním dávkováním bylo nakonec zrušeno. Kombinační léčba byla statisticky významně lepší než sorafenib (HR = 0,78). Všechny podskupiny pacientů měly z léčby benefit. V porovnání samotného durvalumabu se sorafenibem byl rovněž rozdíl v OS, ovšem nebyl statisticky významný (HR = 0,86). Toxicita u sorafenibu byla v mnoha případech vyšší než u použité kombinace a také než u anti‑CTLA‑4 a anti‑PD‑L1.
Z pohledu dlouhodobého sledování ve studii HIMALAYA byl počet pacientů, kteří dosáhli 24měsíčního přežití na kombinaci durvalumab/tremelimumab, 40,5 procenta a těch, kteří dosáhli 36měsíčního přežití na uvedené kombinaci, 30,6 procenta. Tato kombinace prokázala významné zlepšení celkového přežití oproti sorafenibu, což splnilo primární cíl studie, a ukázala, že imunoterapie v první linii má velkou perspektivu. „Studie HIMALAYA je jednou z největších studií fáze III provedených s dlouhodobým sledováním, prokazující roli imunoterapie u chirurgicky neresekabilního HCC,“ zhodnotil MUDr. Kubala.
Další prezentovaná otevřená studie IMbrave150 sledovala léčbu atezolizumab + bevacizumab vs. sorafenib u 501 pacientů s neresekovatelným HCC. Sledovaná kombinace signifikantně zlepšila OS (HR = 0,66). Pokračování studie IMbrave150 u pacientů po progresi ukázalo, že pacienti i po radiologické progresi mají z této léčby prospěch.
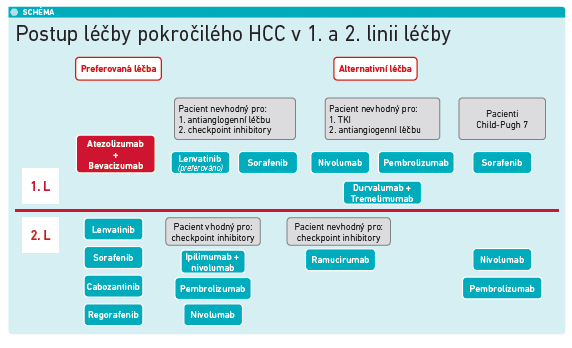
Pro druhou linii léčby HCC byla prezentována studie KEYNOTE‑394 porovnávající léčbu pembrolizumabem vs. placebo. Primárními cíli studie byly OS a PFS, které ukázaly pozitivní statisticky významný výsledek pro pembrolizumab jak v ukazateli OS (HR = 0,79), tak i pro ukazatel PFS (HR = 0,74). Výsledky studie byly celkově konzistentní s výsledky dříve pozorovanými ve studiích KEYNOTE‑224 a KEYNOTE‑240 a podpořily použití pembrolizumabu v léčbě pokročilého HCC ve druhé linii léčby (viz schéma).
Neuroendokrinní tumory
„Podle doporučení ESMO 2020 by měl být u neuroendokrinních tumorů (NET) pankreatu, které jsou nefunkční, tedy hormonálně neaktivní a s velikostí do 2 cm, zvažován konzervativní přístup se sledováním ve specializovaných centrech. U nádorů nad 2 cm je resekce tumoru jednoznačně doporučována,“ uvedl MUDr. Jiří Tomášek z MOÚ Brno. Předmětem studií pak zůstává, zda indikovat k resekci i skupinu NET s velikostí mezi 1–2 cm.
Častou klinickou situaci z praxe, kdy se objevují drobné tumory NET, které jsou resekovány při endoresekci, odrážela multicentrická studie z Jižní Koreje se 346 pacienty stratifikovanými do tří rizikových skupin. Studie ve svém závěru potvrdila dobrou prognózu endoskopických resekci NET rekta, nicméně se vzácnými pozdními relapsy je nutné počítat.
Aktuálně bylo publikováno review ohledně dlouhodobé léčby temozolomidem v souvislosti se sekundárními hematologickými malignitami. Bylo analyzováno 14 studií, v nichž bylo popsáno celkem 25 hematologických malignit, které většinou vznikly až po 12 měsících léčby. Doporučením bylo zhodnotit po šesti měsících efektivitu léčby a po 12 měsících zvážit další podávání temozolomidu.
Nová studie fáze III NETTER‑1 testovala lutecium jako PRRT u pokročilých pacientů s progredujícím midgut tumorem G1, G2. Jako kontrolní léčba byl použit octreotid LAR ve vysokém dávkování 60 mg každé čtyři týdny. Primární cíl studie byl splněn (PFS ve 20. měsíci 65,2 % vs. 10,8 %). Sledovaná léčba byla vysoce bezpečná. Lutecium je oficiálně indikováno k léčbě neresekovatelných nebo metastazujících progresivních a dobře diferencovaných (G1 a G2) gastroenteropankreatických neuroendokrinních nádorů (GEP‑NET), pozitivních na somatostatinový receptor u dospělých pacientů.
Za zmínku stojí probíhající studie fáze III COMPOSE, zaměřená na agresivnější skupiny nádorů G2 a G3 gastroenteropankreatických neuroendokrinních nádorů v 1. a ve 2. linii, nebo studie SWOG S2104 ve fázi II, probíhající u vysoce rizikových neuroendokrinních tumorů po resekci s adjuvantním podáváním kapecitabinu a temozolomidu.
Na závěr své přednášku MUDr. Tomášek komentoval dotazníkové šetření u pacientů s NET (IV. klinické stadium) v USA, kdy se ukázalo, že délka života jako léčebný cíl je nejdůležitější pouze pro 30 procent pacientů. Pro zbývajících 70 procent nemocných je na prvním místě udržení soběstačnosti. Toto šetření u pacientů tedy prokázalo, že udržení nezávislosti je důležitější než samotná délka života.
Kolorektální karcinomy
Problematice kolorektálního karcinomu se zaměřením na imunoterapii se věnoval ve svém sdělení prof. MUDr. Jindřich Fínek, Ph.D., z FN Plzeň. Jako první se zaměřil na nivolumab, molekulu, která se dnes standardně podává u téměř všech solidních nádorů.
V aktuálně probíhající studii CHECKMATE 142 fáze II prokázal nivolumab významnou aktivitu u nestabilních nemocných, tzv. mismatch repair deficientních. Byl podáván ipilimumab standardní dávkou a stejně tak i nivolumab u předléčených nemocných. Hlavním cílem studie byla míra léčebné odpovědi (ORR), která činila 65 procent v průběhu 51 měsíců. U 13 procent pacientů nastala kompletní remise onemocnění. Mediánu doby trvání odpovědi do tří měsíců nebylo dosaženo ve statistické významnosti. „Ve 48 měsících byl čas bez progrese u 53 procent nemocných a 70 procent pacientů přežívalo 48 měsíců, což jsou velmi významná data, ale zatím jen pro malou skupinu pacientů, tzv. MSI‑high, kteří reprezentují měně než 10 procent našich nemocných,“ shrnul závěry studie prof. Fínek.
K dalším významným molekulám patří pembrolizumab, který byl ve fázi III studie KEYNOTE‑177 porovnáván s chemoterapií v kontrolním ramenu v první linii léčby u 307 pacientů MSI‑high kolorektálního karcinomu IV. stadia onemocnění. Medián PFS po léčbě pembrolizumabem byl 16,5 měsíce vs. 8,2 měsíce pro kontrolní léčbu (HR = 0,59), což znamená dvojnásobné prodloužení času do progrese onemocnění po aktivní léčbě. Míra léčebné odpovědi činila 45 procent.
U proficientních pacientů, kteří mají stabilní onemocnění MSI‑high kolorektálním karcinomem, je otázkou, zda jim cílená léčba v kombinací s imunoterapií dokáže pomoci. V prezentované studii fáze II, která zahrnovala 70 pacientů s MSS/pMMR CRC, byl podáván regorafenib s nivolumabem. Medián OS dosahoval 12 měsíců. Další studie sledovala přínos rigorafenibu (80 mg denně) v kombinaci s inhibitorem PD‑1 jakožto záchranné léčby kolorektálního karcinomu (CRC). Ve studii byl zkoumán nový inhibitor PD‑1 sintilimab (200 mg každé 3 týdny) u 24 pacientů s non‑MSI‑high metastatickým CRC. Primárním cílovým ukazatelem studie bylo OS a celková léčebná odpověď na léčbu. Studie má zatím krátkou dobu sledování, medián po pěti měsících léčby se blížil k 17 měsícům, medián času do progrese onemocnění činí 3,1 měsíce.