Inosin pranobex u akutních i chronických virových onemocnění

Léčivý přípravek inosin pranobex (Isoprinosine, IP) byl na světový trh úspěšně uveden před pěti desítkami let. Jeho široké indikace zahrnují akutní i chronické virové infekce bez rozlišení virového kmene. Působí nespecificky, ale rychle a účinně, a to zejména stimulací vzniku a aktivity NK buněk v první ochranné protivirové linii. Doposud publikované výsledky studií ukazují, že IP je účinný nejen u mnoha klasických virových onemocnění, ale i u nových virových nákaz, jako je SARS‑CoV‑2.
Charakteristika přípravku
Inosin pranobex (IP) byl na světový trh byl uveden již v roce 1971 (poprvé v Argentině) a v současnosti je k dispozici ve více než 70 zemích jako antivirotikum s imunomodulačním účinkem. V roce 1982 získal ve Francii Galénovu cenu jako lék roku.1,2 Do současnosti je dostupný pod různými názvy, například Isoprinosine, Immunovir, Viruxan, Virustop, Delimmun apod. Podle Souhrnu údajů o přípravku (SPC) byl schválen k použití v Evropě v prosinci 1981.3
K širokým oficiálně schváleným terapeutickým indikacím patří (podle SPC) 3
- imunodeficitní stavy provázené protrahovanými nebo opakovanými virovými infekty,
- recidivující herpes labialis (HSV‑1) a progenitalis (HSV‑2),
- herpes zoster,li> subakutní sklerotizující panencefalitida – pomalé virové onemocnění, které vzniká důsledkem reaktivity imunitního systému proti spalničkovému viru obvykle v době kdy imunitní systém dozrává,
- cytomegalovirové (CMV) infekce,
- infekce virem Epsteina–Barrové – viróza (EBV),
- condylomata accuminata (genitální bradavice), mukokutánní, vulvovaginální infekce vyvolané lidským papilomavirem (HPV) postihující sliznici děložního hrdla.
Inosin pranobex je v České republice určen k léčbě dospělých a dětí ve věku od jednoho roku. Je považován za lék, který je dobře snášen a nemá závažné nežádoucí účinky. Může se objevit nauzea a diskomfort v oblasti epigastria, bolest hlavy, artralgie, únava.3 Zhruba u 10 % léčených pacientů je pozorováno přechodné a reverzibilní zvýšení koncentrace kyseliny močové v séru a v moči (důsledek metabolismu inosinu jako přirozeného purinu vyskytujícího se v lidském těle).3 V preklinických studiích se též potvrdilo, že IP není cytotoxický, genotoxický ani mutagenní. Od prosince 2019 IP nemá v ČR preskripční ani indikační omezení.
Imunomodulační mechanismy IP (obr. 1)
- Modulace vrozené imunity. IP působí výrazné zvýšení počtu NK buněk již za 90 minut po podání léku a pátý den po prvním podání je počet NK buněk dvojnásobný, IP navíc zvyšuje jejich cytotoxicitu. IP stimuluje buňky prezentující antigen (například dendritické buňky), zvyšuje chemotaxi (makrofágy), zvyšuje expresi receptorů pro složky komplementu a imunoglobulin G (IgG), podporuje fagocytózu.7
- Modulace adaptivní/specifické imunity. IP moduluje maturaci, diferenciaci a cytotoxicitu T lymfocytů adaptivní imunity.5,7 IP zvyšuje produkci interferonu gama, interleukinu 2 (IL‑2) a IL‑10, aktivitu CD4+ T lymfocytů, cytotoxicitu CD8+ T lymfocytů.7
- Homeostatické regulační účinky v zánětu. IP snižuje produkci prozánětlivých cytokinů (TNFα, IL‑6), optimalizuje funkční polarizaci imunoregulačních subsetů T lymfocytů (Th1, Th2, Th17, Treg).7
- Humorální imunitní odpověď. IP zvyšuje protilátkovou odpověď na virovou infekci tím, že stimuluje diferenciaci B lymfocytů na plazmatické buňky, čímž dochází ke zvýšené produkci protilátek.4
- Přímé protivirové působení IP. IP narušuje transkripci virových nukleových kyselin a proteosyntézu virových bílkovin na úrovni tRNA. IP navíc pravděpodobně potencuje specifickou buňkami zprostředkovanou imunitu.7
Reakce imunitního systému na proniknutí viru
První ochrannou bariéru proti virové infekci představuje sliznice s mechanickou ochranou v podobě hlenu a následně nespecifické a specifické mechanismy k likvidaci infekce. Selže‑li tato „první linie“ a replikovaný virus se dostává do mezibuněčných prostor a do krevního oběhu, pak je nastartována kaskáda složitých imunitních dějů, na jejichž konci jsou plazmatickými buňkami (B lymfocyty) produkovány specifické protilátky (IgM, IgG), které se váží na cirkulující virus a snaží se ho tak označit, agregovat, neutralizovat atd.
Pokud je buňka infikována virem, jsou na jejím povrchu exprimovány i fragmenty replikovaného viru. Pak nastupuje role NK buněk (natural killers, tzv. přirození zabíječi), které jsou nejdůležitějšími buňkami v první fázi ochrany před virovou infekcí. Jakmile NK buňky detekují, že je v buňce virus, snaží se buňku zlikvidovat (perforiny a granzymy). NK buňky tak slouží od počátku infekce ke zpomalení rozvoje infekčního procesu, aby mohla být aktivována adaptivní a specifická imunita, která pak infekční proces zastaví.
Zásadní pro ochranu před virovou infekcí a pro její prognózu je dostatečný počet NK buněk v počátcích infekce.5
Role IP v časné reakci imunitního systému
Na rozdíl od specifických antivirotik (protichřipková, antiherpetická) IP aktivuje velmi rychle nespecifickou imunitní odpověď a její protivirovou složku – NK buňky, které účinkují rychle a důsledně.5 V roce 2020 se objevila práce o tom, že IP moduluje buněčnou imunitu indukcí exprese ligandu pro receptor NKG2D na cílových buňkách. NKG2D je aktivační receptor exprimovaný převážně na NK buňkách, CD8+ T lymfocytech, yδ T lymfocytech a některých subsetech CD4+ T lymfocytů.6 Ligandy pro NKG2D jsou exprimovány buňkami, které představují pro organismus nebezpečí – infikované buňky, buňky s poškozenou DNA, nádorové, senescentní buňky apod. IP pomáhá „zviditelňovat“ tyto ligandy pro buňky imunitního systému, včetně NK buněk.
Prokázané a možné mechanismy účinku IP popisuje podrobně Jan Krejsek (2018).7 Z uvedeného vyplývá, že účinky IP jsou pleiotropní, IP působí na mnoha úrovních imunitního systému a pozitivně moduluje jeho aktivitu.1,4,6,7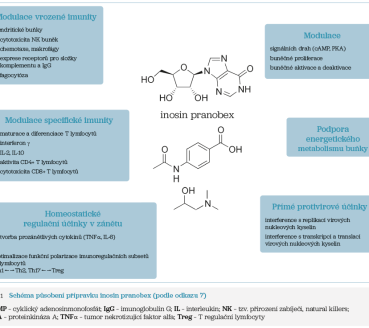
Inosin pranobex v klinické praxi
Inosin pranobex byl zkoumán od svého objevení do současnosti ve stovkách klinických studií.
Jaromír Bystroň8 upozorňuje v široce koncipovaném článku Často nemocné dítě na možné příčiny častých infektů u dětí, kde jako jedno z řešení může být zvolena imunomodulační léčba IP.
Zuzana Humlová9 v článku Prolongované stavy nemocnosti a vracející se infekce v ordinaci praktického lékaře řadí k vhodným indikacím IP herpetické infekce (opary rtů či genitálu způsobené HSV‑1, resp. HSV‑2), cytomegalovirové infekce, onemocnění vyvolaná virem Epsteina–Barrové. Velmi přínosnou je léčba IP afekcí způsobených lidskými papilomaviry (onkogenními i vyvolávajícími genitální bradavice v kombinaci s lokální terapií).
Multicentrická randomizovaná studie, která porovnávala účinnost IP (4 g denně) oproti acikloviru v léčbě opakovaných oparů (herpes labialis, herpes progenitalis), prokázala stejný klinický efekt obou léčiv na akutní stav a v případě skupiny IP navíc významně nižší četnost exacerbace oparů v období tří měsíců po ukončení léčby.10
Randomizovaná, dvojitě zaslepená multicentrická studie fáze IV sledovala 463 jedinců s respiračním onemocněním, kterým byl podáván IP (n = 231) nebo placebo (n = 232). K ústupu všech příznaků a ke zlepšení došlo rychleji ve skupině léčené IP než ve skupině s placebem.11
Isoprinosine proti covidu‑19? Proč ne!
V době pandemie SARS‑CoV‑2 vzbudila pozornost česká retrospektivní studie, která hodnotila úmrtnost na SARS‑CoV‑2 ve třech domech s pečovatelskou službou v období od června do září 2020.12 V celé kohortě 301 seniorů ve věku 65 až 85 let a starších užívajících IP byla významně snížena smrtnost (case fatality rate) v porovnání s jinými pečovatelskými domy (OR = 2,8). Podle autorů byl účinek IP významný, nicméně se jedná o předběžné výsledky, které vyžadují rozsáhlejší prospektivní studie u pacientů s covidem‑19.
Časopis Advanced Therapeutics13 uveřejnil výsledky prospektivní multicentrické dvojitě zaslepené a placebem kontrolované studie fáze III, která hodnotila účinnost a bezpečnost IP u 416 pacientů s potvrzeným mírným až středně těžkým onemocněním covid‑19. Kromě definované standardní péče byli pacienti randomizováni (1 : 1) k léčbě IP v dávce 50 mg/kg tělesné hmotnosti/den (maximálně 4 g denně) podávané ve 3–4 dílčích dávkách po dobu 10 dnů nebo k aplikaci placeba. Ve srovnání s placebovou skupinou vykázala skupina nemocných léčená IP významně vyšší míru klinické odpovědi a klinického vyléčení v šestém dni jak u nehospitalizovaných pacientů, tak u celé populace. Ve skupině s IP nedošlo k úmrtí po dobu sledování (14 dní), zatímco v placebové skupině zemřeli za sledované období dva nemocní. Nebyly zaznamenány žádné neznámé nežádoucí účinky IP, bezpečnostní profil byl konzistentní s výsledky předchozích studií s IP.
Autoři upozorňují, že vzhledem k mechanismu účinku IP by měla být léčba zahájena co nejdříve po prvních příznacích. (Registrační číslo studie CTRI/2021/02/030892). Výsledky studie dobře dokumentuje graf 1a, b.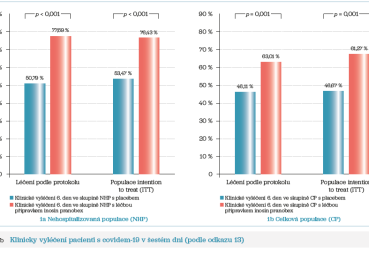
Závěr
Vzhledem k prokázaným imunomodulačním a antivirovým účinkům a bezpečnostnímu profilu je inosin pranobex vhodný k léčbě širokého spektra virových infekcí a z nich vyplývajících onemocnění, včetně subakutní sklerotizující panencefalitidy, herpetických obtíží, důsledků infekce lidskými papilomaviry, chřipky a cytomegalovirových infekcí a infekcí virem Epsteina–Barrové. Nově publikovaná prospektivní randomizovaná studie prokazuje efekt IP i u pacientů s covidem‑19. Inosin pranobex spojuje vlastnosti antivirotika a podpory imunitních obranných reakcí.
Literatura
- Bystroň J. Isoprinosine a imunitní systém – důkazy o imunomodulačním účinku. XXXVII. ČSAKI, 2020.
- Bystroň J. Isoprinosine (inosin pranobex) – od experimentu ke klinické zkušenosti. Alergie 2020;2:127–133.
- Isoprinosine. Souhrn údajů o přípravku. SÚKL. Poslední revize 2018.
- Slíva J, et al. Inosin pranobex: klíčový lék v boji proti široké škále virových infekcí a neinfekčních nemocí. Adv Ther 2019;36:1878–1905.
- Beran J. Inosin pranobex a jeho možnosti v prevenci a v léčbě akutní respirační virové infekce včetně COVID‑19 – odpovědi na dotazy zdravotnických pracovníků. Pro Lékaře. Meditorial. 24. 3. 2020.
- McCarthy MT, et al. Inosine pranobex enhances human NK cell cytotoxicity by inducing metabolic activation and NKG2D ligand expression. Eur J Immunol 2020;50:130–137.
- Krejsek J. Inosin pranobex, klinickou praxí ověřený účinný imunomodulátor; možné mechanismy působení. Remedia 2018;28:396–400.
- Bystroň J. Často nemocné dítě. Pediatr praxi 2020;21:163–166.
- Humlová Z. Prolongované stavy nemocnosti a vracející se infekce v ordinaci praktického lékaře. Med praxi 2020;17:260–263.
- You Y, et al. Multicenter randomized study of inosine pranobex versus acyclovir in the treatment of recurrent herpes labialis and recurrent herpes genitalis in Chinese patients. J Dermatol 2015; 42: 596–601.
- Beran J, et al. Inosine pranobex is safe and effective for the treatment of subjects with confirmed acute respiratory viral infections: analysis and subgroup analysis from a Phase 4, randomised, placebo‑controlled, double‑blind study. BMC Infect Dis 2016;16:648.
- Beran J, et al. Inosine Pranobex Significantly Decreased the Case‑Fatality Rate among PCR Positive Elderly with SARS‑CoV‑2 at Three Nursing Homes in the Czech Republic. Pathogens 2020;9:1055; doi:10.3390/pathogens9121055.
- Jayanthi CR, et al. Efficacy and Safety of Inosine Pranobex in COVID‑19 Patients: A Multicenter Phase 3 Randomized Double‑Blind, Placebo‑Controlled Trial. Adv Therap 2022;2200159.