Dyslipidémie v pediatrické praxi

V bloku ICHS na odborném setkání 34. Šamánkovy Poděbrady vystoupil prof. MUDr. Michal Vrablík, Ph.D., ze III. interní kliniky 1. LF UK a VFN Praha s přednáškou o dětských poruchách lipidového spektra a o současných i budoucích možnostech jejich řešení.
Ateroskleróza je důležitá, ale není jedinou cévní patologií. „Všichni máme aterosklerózu, ale většině z nás nevadí, protože je ještě v časných, dobře ovlivnitelných stadiích. V zásadě se jí bát nemusíme, pokud máme nízké koncentrace aterogenních lipoproteinů, ovšem není to jen LDL částice, která dokáže vnést cholesterol do naší cévní stěny,“ uvedl prof. Vrablík. Například problematika chronického srdečního selhání (CHSS) je pravděpodobně lipidy ovlivnitelná pouze v rámci preventivních opatření, ale při jeho manifestaci se managementem dyslipidémie prognóza nemocných s CHSS příliš ovlivnit nedá.
Proč se v dětském věku zabývat cholesterolem?
Čerstvých dat a klinických důkazů ohledně rizikovosti koncentrace cholesterolu v pediatrické praxi je v této oblasti velmi málo, neboť chybějí epidemiologická šetření. „Dokonce vůbec nevíme, jaká je normální požadovaná vhodná koncentrace sérových lipidů u dětských pacientů,“ poznamenal prof. Vrablík.
Geneticky naprogramovaní jedinci, kteří celoživotně žijí s nižší než průměrnou populační koncentrací aterogenních lipidů, mají celoživotně dramaticky snížené riziko cévních komplikací. Na každý 1 mmol/l snížení LDL‑C připadá 50procentní redukce relativního rizika ICHS, což je dvojnásobek redukce rizika, které je možné dosáhnout farmakologickou intervencí v pozdějším věku. Je známo, že kumulace rizikových faktorů a krevního tlaku v mladším věku je významnější pro budoucí manifestaci časných komplikací aterosklerózy, než když dochází k této kumulaci rizika ve věku pozdějším. Největší význam z hlediska prognostického ovlivnění má tedy zaměření na mladší věkové kategorie mezi 30–40 lety věku, kde je žádoucí toto riziko detekovat a snažit se je modifikovat.
Dalším důvodem, proč se v pediatrii zabývat dětskou dyslipidémií, je skutečnost, že tato porucha má z 90 procent genetický základ. Odborníky v současné době nejvíce zajímají monogenní formy závažných familiárních dyslipidémií, především familiární hypercholesterolémie (FH). Jedná se o onemocnění, které je nejčastější vrozenou poruchou metabolismu s prevalencí 1 : 200.
Familiární hypercholesterolémie (FH) je v dětském a adolescentním věku zvláště důležitá, protože ve věku 25–39 let je pro jejího nositele riziko infarktu myokardu zvýšeno 20–30krát. Dokonce mezi 20. a 30. rokem věku ve srovnání s referenční populací jsou nositelé FH ve stonásobně vyšším riziku infarktu myokardu, což je dáno také faktem, že takto mladá populace zdravých jedinců má obecně velmi nízké riziko pro rozvoj těchto pokročilých cévních komplikací (Benn et al., J Clin Endocrinol Metab. 2012;97(11):3956–3964).
Z výše uvedeného vyplývá zásadní otázka: kdo a kdy má diagnostikovat a léčit dyslipidémie. Pokud je zásadní včasný zásah, tak pro naplnění uvedeného požadavku by hledaným lékařem měl být pediatr. Ten by měl bezpochyby rozpoznat vrozené monogenně podmíněné dyslipidémie, a to nejen FH, ale i další poruchy, a ty by měly být sledovány již od dětského věku.
V České republice je zaveden selektivní screening familiární dyslipidémie dětí v pátém a třináctém roce věku. Právě v postižených rodokmenech má být vyšetřen lipidogram. Pro uvedené pacienty jsou v České republice specifická centra MedPed, která mají 15 pediatrických odnoží pokrývajících celou republiku. Díky nim existují informace o 10 000 nositelích FH, což je asi pouze 25 procent předpokládaného počtu všech pacientů s FH. Nicméně i tak uvedené procento řadí Českou republiku na třetí nejlepší místo v Evropě.
Projekt CzeCH‑IN
Pro zvýšení podílu zachycených pacientů s FH byl v ČR spuštěn pilotní projekt univerzálního screeningu FH pod názvem CzeCH‑IN (Check Cholesterol in Newborns in the Czech Republic). Projekt má za cíl prokázat, zda by bylo možné zjistit a diagnostikovat spolehlivě FH vyšetřením cholesterolu v pupečníkové krvi. Pupečníková krev je totiž snadněji dostupný materiál než jakýkoli jiný materiál dosažitelný později během života dítěte. Navíc pro získání pupečníkové krve neexistuje příliš velká bariéra, která pravděpodobně limituje pozdější selektivní screening, tj. ochotu rodičů nechat testovat své malé děti. Projekt CzeCH‑IN má ambici vyšetřit deset tisíc novorozenců, aktuálně je vyšetřeno přes pět tisíc dětí. Plán projektu stanovuje vyšetření celkového cholesterolu a LDL‑C u všech respondentů. Navíc u těch osob, které budou nad 85. percentilem distribuce, bude provedena kompletní genetická analýza.
Hlavním cílem projektu CzeCH‑IN je nalézt nejefektivnější kombinace biochemické a molekulární diagnostiky pro stanovení diagnózy FH u novorozenců a dále zjistit, zda je novorozenecký screening FH efektivním a realizovatelným způsobem univerzálního či celoplošného screeningu. Na základě statistických údajů se předpokládá, že ze 110 000 novorozenců se každý rok narodí asi 400 nových nositelů onemocnění FH. V případě, že je tímto způsobem identifikováno dítě a rodič není rozpoznán, což se bohužel děje často, je šance provést reverzní kaskádový screening – tedy jít dál ke starším rodinným příslušníkům, a tak odhalit i dospělé nositele tohoto onemocnění.
V zahraničí jsou preferovány odlišné formy univerzálního screeningu FH založené na technice POCT (Point of Care Testing), což je vyšetření pacienta na místě, tj. přímo v ordinaci. Ambulantní lékaři v České republice poměrně často používají přímo ve svých ordinacích různé vyšetřovací metody, např. stanovení CRP, a mají tak svoji „malou laboratoř“ po ruce. Tuto laboratoř v ordinaci by bylo možné rozšířit o lipidový panel. „Bohužel standardizace a citlivost těchto metod POCT pro vyšetření lipidogramu není zcela optimální, a navíc toto vyšetření není levné,“ komentoval prof. Vrablík s tím, že existuje bariéra vyplývající ze skutečnosti, že v České republice je poměrně hustá síť stacionárních laboratorních pracovišť, takže řada biochemiků přístup POCT pro stanovení lipidů pokládá za zbytečný, a navíc upozorňují na technické nedokonalosti stanovení lipidů přímo v ordinacích. Na druhou stranu by POCT mohl odstranit překážku, kdy lékař identifikuje potenciálně rizikové dítě a odešle jej k odběrům do laboratoře. Ve většině případů se však finální odběr neuskuteční, neboť rodič pokládá toto vyšetření za nadbytečné a rozhodne se odběr s dítětem neabsolvovat.
Specificita a senzitivita vyšetření lipidů v různých věkových kategoriích ukazuje, že v tomto ohledu je novorozenecká kategorie hned druhá nejvhodnější. Ideální je však vyšetřovat lipidy u dětí ve věkovém rozmezí pátého až devátého roku věku, kde je specificita a senzitivita stanovení nejlepší.
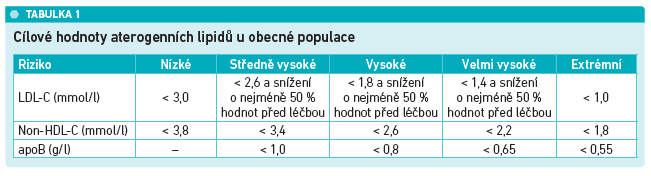
Cílové hodnoty plazmatických lipidů u obecné populace
Dle nových doporučených postupů ESC/EAS z roku 2019 se cílové hodnoty vyšetření plazmatických lipidů u obecné populace neustále zpřísňují. Stanovují se především koncentrace LDL‑C, non‑HDL‑C a apoB, které jsou z hlediska managementu lipidů na prvním místě důležitosti sledování (viz tabulku). Poslední dva jmenované parametry jsou přesnější u nemocných s inzulinovou rezistencí a diabetem, u kterých dochází ke kumulaci aterogenních non‑LDL částic.
Farmakoterapeutická opatření pro management dyslipidémie se v průběhu let neustále rozšiřují, což se týká především dospělé populace pacientů, nicméně statiny, ezetimib, a dokonce i nejmodernější léčba mají důkazy o svém účinku a bezpečnosti i v pediatrické populaci. Farmakoterapie dyslipidémie u dětí je rezervována pro nositele familiárních forem, především FH. Dle doporučených postupů pro léčbu dětské populace platí cílová hodnota LDL‑C pod 3,5 mmol/l. Statistiky uvádějí, že dětští pacienti s poruchou FH mají před léčbou průměrnou vstupní hodnotu LDL‑C nad 5 mmol/l.
Klinické důkazy pro léčbu dyslipidémie u dětí
Přestože zatím neexistují mortalitní data, která by ukázala, že léčba statiny u dětské populace snižuje mortalitu, ukazuje se, že včasná intervence u této skupiny dětských pacientů má značný význam. Jak prof. Vrablík uvedl, 20letá data z Nizozemska pro podávání statinů u dětí dokumentují, že ve srovnání s rodiči dětí, kteří žili před érou statinů, tyto děti mají významně nižší, prakticky chybějící výskyt cévních příhod ve stejném věku, kterého se nyní dožívají při léčbě zavedené mezi šestým a osmým rokem věku (Luirink IK et al., N Engl J Med. 2019;381(16):1547–1556). Hypolipidemická farmakoterapie u dětí má své místo pouze ve vymezených případech a měla by být v rukou zkušených specialistů.
Kromě statinů lze u dětí podávat i nejmodernější hypolipidemickou terapii, pro kterou aktuálně existují klinické důkazy. K dispozici je biologická léčba využívající monoklonálních protilátek nebo oligonukleotidových sekvencí různého uspořádání, kterými je ovlivňován protein PCSK9. „Protilátky proti tomuto proteinu přidají k efektu statinu další 50procentní redukci LDL‑C, což finálně vyústí v následný 15procentní pokles cévního rizika, jak dokumentovaly velké klinické studie s inhibitory PCSK9 evolokumabem a alirokumabem,“ zdůraznil prof. Vrablík (Sabatine MS et al., N Engl J Med. 2017;376(18):1713–1722). Oba tyto inhibitory PCSK9 byly zvažovány i k použití u pediatrických populací a první práce, která postulovala algoritmus pro nejvíce ohrožené nositele FH, doporučila zvážit používání inhibitorů PCSK9 u pacientů od 16–18 let věku (Vuorio A et al., Eur Heart J. 2016;37(17):1353–1356). Na základě uvedeného postulátu byly uspořádány a provedeny klinické pediatrické studie (ODDYSEY KIDS, HAUSER‑RCT) s oběma uvedenými přípravky, které následně prokázaly jejich účinnost a bezpečnost. Do uvedených studií byly zařazeny děti s diagnózou FH ve věku 8–17 let. Data pro redukci rizika cévních příhod po použití inhibitorů PCSK9 zatím u dětské populace k dispozici nejsou, neboť doba klinického používání inhibitorů PCSK9 je příliš krátká.
Hudba blízké současnosti
Jedná se o terapie, které využívají modifikace přenosu genetické informace z DNA až k proteinu, většinou na úrovni translace, tedy na úrovni přepisu messengerové RNA (mRNA) do sekvence aminokyselin. Uvedených možností existuje celá řada. Nejpokročilejší z nich je terapie pomocí tzv. siranu, což je oligonukleotidová sekvence dvoušroubovice komplementární s vybraným cílovým genem, jehož translaci je potřeba inhibovat. V tomto případě se jedná opět o gen pro PCSK9.
První z kategorie siranů je inklisiran, který je modifikovanou oligonukleotidovou sekvencí, která má rezistenci vůči endo‑ a exonukleázám, a má tedy dlouhou biologickou životnost (Ray et al., N Engl J Med. 2020;382(16):1507–1519). Inklisiran je specificky upraven, takže má jasnou hepatoselektivitu. V hepatocytu inklisiran ovlivní intracelulárně translaci proteinu s délkou působení účinku šest měsíců. Podávaný ambulantně jednou za půl roku snižuje koncentraci LDL‑C o 50 procent. V České republice je léčba inklisiranem již registrována a aktuálně probíhá úhradové jednání.
Hudbou zřejmě vzdálenější budoucnosti bude pravděpodobně možnost tzv. genové editace pomocí systému CRISPR PCSK9, objevenou americkými vědkyněmi, které byly za tento počin oceněny Nobelovou cenou. „Jedná se o vypnutí genetické informace, kterou považujeme za nepotřebnou, nebo té, která je nesprávná,“ přiblížil tento princip prof. Vrablík. Využitím uvedeného modelu při cílení na gen pro PCSK9 lze natrvalo odstranit PCSK9, a tím snížit koncentrace LDL‑C až o 50 procent. Experiment byl zatím proveden pouze u zvířat, a to konkrétně u makaků (Musunuru K et al., Nature. 2021;593(7859):429–434). Zda tento přístup bude aplikovatelný do budoucna i u člověka, je zatím otázkou, neboť systém CRISPR PCSK9 zatím nefunguje dostatečně přesně. „Vypnutí genu PCSK9 pravděpodobně není spojeno s dalšími nežádoucími účinky, nicméně mohlo by se stát, že bychom současně s tímto genem mohli vypnou i genovou informaci kousek vedle, která by nám pak mohla chybět, což uvedený přístup limituje,“ uzavřel své sdělení prof. Vrablík.