Srdeční selhání 2024 – léčba bez hranic
Kardiovaskulární (KV) onemocnění jsou v Česku stále dominantní příčinou morbidity a mortality. Tento neblahý trend ale začíná být tažen především jednou diagnózou, srdečním selháním (SS). Aktuálně se se SS léčí zhruba 380 000 pacientů, a pokud se nic nezmění v oblasti prevence, jsou predikce neúprosné – v roce 2040 by v České republice mohlo být až 900 000 osob se SS. Je proto nejvyšší čas, že čeští kardiologové přicházejí se strategickým plánem, jak nárůst SS v populaci výrazně zpomalit. Zásadně pomoct jim může i nová terapie, která v klinických studiích prokázala, že je schopna „měnit pravidla hry“.
Srdečnímu selhání se velmi komplexně věnovalo dvoudenní březnové sympozium společnosti Boehringer Ingelheim s názvem Srdeční selhání bez hranic, a to za účasti špiček české kardiologie. Další přední odborníci se pak podíleli na sérii osmi workshopů, které se zabývaly především mezioborovými souvislostmi.
Národní kardiovaskulární plán cílí na slabiny kardiologické péče
Odborný garant sympozia a místopředseda České kardiologické společnosti prof. MUDr. Aleš Linhart, DrSc., v prvním sdělení připomněl, že díky Národnímu kardiovaskulárnímu plánu z roku 2013 se českým kardiologům podařilo konsolidovat systém akutní kardiologické péče, který dnes dosahuje těch nejlepších výsledků v mezinárodním srovnání. Připustil ale, že problémy stále přetrvávají v oblasti péče o chronická KV onemocnění, která jsou stále dominantní příčinou nemocnosti a úmrtnosti v ČR. Největší hrozbou se ukazuje být právě SS. „V přesném odhadu nás trochu brzdí systém MKN, protože diagnóza srdeční selhání často není primární diagnózou – řada pacientů ji nemá vykázánu, ale mají nějaké kardiovaskulární onemocnění, které může být se srdečním selháním spojeno. Pokud vyjdeme z tohoto předpokladu, je predikce počtu pacientů se srdečním selháním závratná,“ uvedl prof. Linhart. Podle dat NRHZS z let 2010–2022 je kumulativní počet pacientů s historií léčby SS přibližně 380 000. Pokud se nic nezmění, do roku 2040 v Česku bude 800 000 až 900 000 osob se SS, což představuje enormní zátěž pro zdravotnictví i ekonomiku země. Od roku 2010 začíná SS také dominovat jako příčina úmrtnosti u mužů i žen. V roce 2021 zemřelo v ČR na srdeční selhání 8 783 osob (83,5 na 100 000 obyvatel). Nárůst je dán jednak lepší diagnostikou SS, ale pochopitelně i rostoucí incidencí SS v důsledku stárnutí populace a výskytu komorbidit, kterých je s SS spojena celá řada. „Jde o obtížně řešitelný problém, navzdory dostupnosti moderních a účinnějších léků. Se stárnutím mnoho neuděláme,“ podotkl prof. Linhart. Přesto se čeští kardiologové nevzdávají a loni připravili nový Národní kardiovaskulární plán pro roky 2023–2033, který má vizi zajistit každému obyvateli České republiky možnost prevence vzniku kardiovaskulárního onemocnění a v případě jeho rozvoje zajistit nejvyšší možnou kvalitu péče a života bez ohledu na geografickou polohu či stadium nemoci. Jinak řečeno, nový plán chce cílit na primární prevenci, a to již od školních let, a tam, kde se KV onemocnění nepodaří zabránit, chce zajistit co nejlepší podmínky pro kvalitní následnou péči zabraňující vzniku dalších komplikací. Plán, který by letos na jaře měla jako strategický dokument schválit vláda, počítá s rozvojem a kultivací specializovaných kardiologických pracovišť, např. právě pro léčbu SS, ale jeho tvůrci si uvědomují, že slabinou jsou a budou regionální nerovnosti v distribuci specializovaných ambulancí. Tady budou muset kardiologům pomoci zdravotní pojišťovny a ministerstvo, ale i místní samosprávy. „Pacient se srdečním selháním je komplikovaný pacient, který vyžaduje hodně času a prostředků. Kardiologové na péči o tyto nemocné zatím prodělávají. I to se tedy musí změnit,“ zdůraznil prof. Linhart a dodal, že kardiologický plán se bude snažit také o vymezení fungující spolupráce s praktickými lékaři. Žádné systematičtější změny nejsou možné bez kvalitních dat – je proto dobrou zprávou, že v loňském roce se začala data otevírat a byl spuštěn Národní kardiologický informační systém (NKIS), který nabízí data o morbiditě a mortalitě. „Povzbudivé je, že se nám daří v léčbě srdečního selhání zavádět léčbu založenou na důkazech. Naším cílem je, aby pacienti se srdečním selháním dostali léčbu inhibitory SGLT‑2, neboť ta významným způsobem zlepšuje symptomatologii a redukuje hospitalizace pro srdeční selhání, což je velice důležité pro prognózu pacientů,“ řekl (viz graf).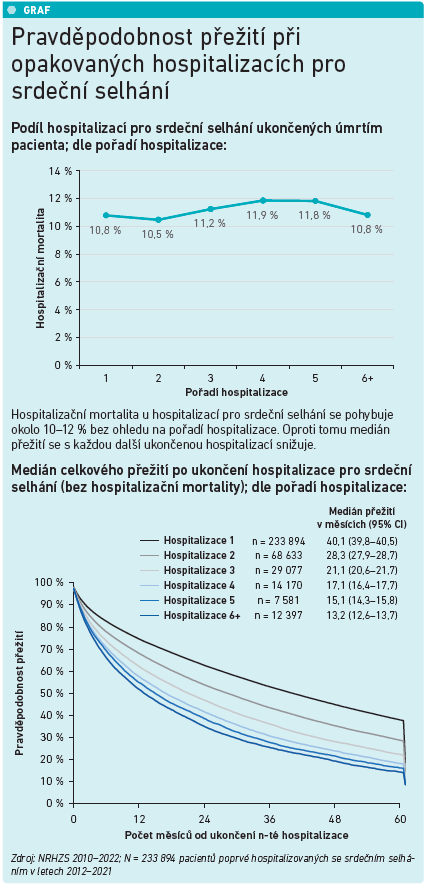
Prof. Linhart se v závěru svého sdělení dotkl problematiky SS se zachovanou ejekční frakcí (HFpEF). Zdůraznil, že v klinické praxi je třeba dobrat se diagnózy z hlediska etiologie, což se ne vždy daří. Původem HFpEF může být arteriální hypertenze, ICHS, diabetická kardiomyopatie, amyloidóza, renální selhání, ale i např. zvýšená tepenná tuhost, restriktivní kardiomyopatie či kardiotoxická léčba (Anker et al., Eur J Heart Fail. 2023). Patofyziologickým mechanismem může být systémový zánět, ischémie myokardu, apoptóza a fibróza, hypertrofie, abnormální využití energie, porucha signalizace atd., ať už se jedná etiologicky o postižení v důsledku hypertenze, metabolického syndromu, nebo ICHS. Při HFpEF dochází k remodelaci myokardu a rozvoji dysfunkce na úrovni relaxace, na úrovni compliance, klesá inotropie a chronotropie, mění se hemodynamika (zvýšení plnicích tlaků levé komory, snížení orgánové perfuze), což nakonec vede k tomu, že pacienti mají manifestní SS. Inhibitory SGLT‑2 podle prof. Linharta představují průlom – léčebnou modalitu, která prokazatelně zlepšuje prognózu pacientů s HFpEF. „Přímo dochází k ovlivnění metabolických vlastností myokardu a zlepšení využitelnosti energie v myokardu. Mírná ketonémie navozená inhibitory SGLT‑2 znamená přísun energie strádajícímu srdečnímu svalu. Vidíme tu ale i spoustu nepřímých efektů, např. renoprotektivních, antioxidačních, dochází ke snížení koncentrací kyseliny močové a zvýšení erytropoetinu. Víme, že tento multifaktoriální mechanismus funguje a vede ke zlepšení prognózy nemocných zcela významně,“ shrnul prof. Linhart. Jeden z výsledků studie EMPEROR‑PRESERVED u pacientů s mírně sníženou nebo zachovanou ejekční frakcí (Butler et al., Circulation 2022) navíc prokázal při léčbě empagliflozinem také zlepšení kvality života dle Kansas City Cardiomyopathy Questionnaire (KCCQ). „Glifloziny fungují napříč spektrem ejekční frakce, tedy bez hranic. Možná časem dojde i k tomu, že se nebude srdeční selhání rozlišovat podle ejekční frakce, ale podle zcela jiných kritérií,“ uzavřel prof. Linhart.
Epidemiologie SS a možnosti programu VZP PLUS pro srdeční selhání
Prof. MUDr. Miloš Táborský, CSc., přednosta I. interní kliniky – kardiologické LF UP a FN Olomouc, konstatoval, že ač např. dánský registr (Christiansen, Circulation 2017) ukazuje, že spolu se zavedením moderní léčby SS začíná nastupovat trend poklesu jednoroční mortality u pacientů s nově diagnostikovaným SS, je varující, že se SS začíná objevovat u mladších osob. Pokud se tedy v ordinaci objeví čtyřicátník či padesátník, který je dušný a má možnou symptomatologii SS, je třeba tomu včas věnovat pozornost.
Pokud jde o epidemiologii SS v ČR, nejsou data podle prof. Táborského úplně dokonalá. Přesto se lze dostat k poměrně realistickým číslům. Práce Táborský M et al. (ESC Heart Failure 2021) ukazuje vývoj prevalence SS mezi lety 2012 a 2018. Za tuto dobu došlo k výraznému nárůstu počtu osob s SS (ze zhruba 180 000 na 286 000). ÚZIS ČR poskytl odhad vývoje prevalence chronického SS v ČR mezi lety 2012 a 2023. Jak popsal už prof. Linhart, tendence je rostoucí a převažujícím fenotypem je HFpEF. SS je typicky nemoc vyššího věku, prakticky všichni pacienti mají hypertenzi, dvě třetiny mají ICHS, přes 60 procent má arytmie, 50 procent fibrilaci síní (FS), polovina má dyslipidémii, 40 procent diabetes (Táborský et al., Biomedical Papers 2021). „Diabetici tvoří významnou skupinu pacientů se srdečním selháním, současně ale nejvíce profitují z moderní terapie inhibitory SGLT‑2,“ podtrhnul prof. Táborský. SS je také třetí nejčastější kardiovaskulární příčinou úmrtí, po ICHS a cévních onemocněních mozku (NRHZS 2022). Stejně jako pro infarkt myokardu je i pro SS výrazná krajová diference – nejvíce léčených pacientů se SS měl v roce 2022 na 100 000 obyvatel Plzeňský kraj, následoval kraj Liberecký a Karlovarský.
Hospitalizační (30denní) mortalita by se měla v posledních letech díky zavedení moderní terapie snižovat. V ČR v roce 2022 zemřelo na SS při hospitalizaci (do 30 dní od přijetí) 4 041 pacientů, což je 10,7 procenta ze všech pacientů hospitalizovaných pro SS.
„Na sledování změny trendu je potřeba ještě vyčkat, zavedení moderní terapie se neprojeví hned, má určitou setrvačnost,“ komentoval poslední dostupná data prof. Táborský. Dodal, že exaktní epidemiologická data o zastoupení fenotypu HFpEF v populaci nejsou k dispozici, předpokládá se ale prakticky stejný počet pacientů jako nemocných fenotypu HFrEF. Incidence i prevalence HFpEF narůstá v důsledku stárnutí populace, vysokého výskytu obezity, hypertenze, sedavého životního stylu a zejména diabetu. Pacienti s HFpEF jsou v porovnání s pacienty HFrEF vyššího věku, častěji jde o ženy. Tito nemocní mají více kardiálních i nekardiálních komorbidit (FS, renální insuficience, CHOPN atd.). Morbidita a mortalita pacientů s HFpEF je v průběhu sledování vysoká, podobná pacientům s HFrEF. Rozdíl proti HFrEF však spočívá v tom, že hospitalizace a úmrtí u pacientů s HFpEF mají častěji nekardiální příčiny. Jak je známo, každá rehospitalizace pro dekompenzaci chronického SS je významným negativním prognostickým ukazatelem. Až 20 procent pacientů propuštěných z nemocnice je znovu přijato do 30 dnů, 50 procent je pak znovu přijato do šesti měsíců (Khan et al., Circ Heart Fail. 2021). „Inhibitory SGLT‑2 je možné podat časně, už na konci hospitalizace. Tato včasná léčba má význam v prevenci rehospitalizací,“ zdůraznil prof. Táborský.
Péče o narůstající počet pacientů se SS je náročná. Proto je od 1. ledna 2024 pro kardiology dostupný motivační program VZP PLUS Kvalita péče o pacienty s chronickým srdečním selháním. Má za cíl motivovat poskytovatele, kteří mají ve své péči pojištěnce s chronickým SS, k zajištění kvalitní péče o dispenzarizované pacienty. „Tyto programy pomáhají zvládat zátěž ambulancí pacienty se srdečním selháním, podporují správnou medicínskou praxi a umožňují předpis inovativních molekul dle doporučených postupů – bez vlivů na průměrný náklad na pacienta. Ambulanci přinášejí aditivní finanční prostředky nad rámec vykazovaných či uznaných výkonů,“ shrnul benefity programu prof. Táborský. Doplnil, že program sleduje tři parametry – podíl dispenzarizovaných pacientů se SS s optimální maximálně tolerovanou farmakoterapií SS vztažený ke všem dispenzarizovaným pacientům se SS na daném pracovišti, podíl dispenzarizovaných pacientů se SS s provedeným komplexním echokardiografickým vyšetřením minimálně 1× ročně vztažený ke všem dispenzarizovaným pacientům se SS na daném pracovišti a podíl dispenzarizovaných pacientů se SS s monitorací natriuretických peptidů (vyšetření NT‑proBNP nebo BNP v laboratoři minimálně 1× ročně). Aktuálně má dodatek na VZP PLUS podepsáno 259 poskytovatelů odbornosti 107, tj. asi 80 procent všech ambulantních kardiologů.
„Chronické srdeční selhání je nadále závažným problémem, nicméně díky inovativním terapiím v oblasti jak farmakologické, tak nefarmakologické máme šanci snížit mortalitu, morbiditu a zlepšit kvalitu života těchto nemocných. Kromě dobře zvládnuté problematiky srdečního selhání se sníženou ejekční frakcí musíme stále více pozornosti věnovat problematice zachované ejekční frakce. Využívejme k tomu na maximum programu VZP PLUS pro srdeční selhání ve prospěch našich pacientů,“ uzavřel prof. Táborský.
Simulační worshopy a jejich využití v ambulanci srdečního selhání
S významem a průběhem tzv. simulačních workshopů seznámil přítomné kardiology prof. MUDr. Jan Bělohlávek, Ph.D., z II. interní kliniky – kliniky kardiologie a angiologie 1. LF UK a VFN Praha, který se profesně věnuje akutní kardiologii. Na úvod zdůraznil, že simulačním kursem by měl projít každý lékař a zdravotník, protože jeho cílem je vyhnout se zmatku ve chvílích, kdy je třeba efektivně komunikovat v týmu a jednat podle určených rolí. Podle jeho slov je v akutních situacích klíčová právě komunikace, a to ve všech fázích náhlé situace. „Smyslem není vyzkoušet si nějakou technologii či techniku, ale vyzkoušet si a natrénovat komunikaci v týmu týkající se předání pacienta a všech informací o něm, rychlého vyšetření a zhodnocení stavu. Je důležité si natrénovat orientaci v situaci, schopnost naplánovat činnosti a rozdělit role v týmu včetně role vedoucí,“ specifikoval prof. Bělohlávek. Simulační kursy či workshopy se odehrávají v realistickém prostředí, což jim dodává potřebnou věrohodnost. Výkony se provádějí rovněž reálně, nejde o demonstrace. Další výhodou kursu je bezpečné prostředí, které dovoluje chyby, a následně poskytnutý debriefing, tedy čas na reflexi a rozebrání situace v týmu. „Simulace probíhají s cílem zvyšovat bezpečnost a kvalitu zdravotní péče, nejde primárně o rozvoj nějakých technických dovedností, ale dovedností netechnického typu,“ doplnil prof. Bělohlávek a přirovnal simulace v medicíně k simulacím v leteckém průmyslu, které se zaměřují na souvislosti, standardní znalosti, praktické dovednosti a CRM, tj. Crew/Crisis Resource Management. Medicínské simulace by měly probíhat systematicky, postupně, opakovaně (aspoň 2× ročně) a měly by zahrnovat celý tým daného oddělení, tedy včetně sester. Lektor simulačního kursu nemusí být nutně lékař.
Nový věstník MZ ČR 3/2024 podporuje simulační kursy, konkrétně simulace kritických stavů ve všech základních i specializovaných oborech – nově tedy simulačním kursem projdou povinně všichni lékaři, kteří budou podstupovat nějakou atestaci.
Fenotypy a diagnostika HFpEF
Prof. MUDr. Jan Václavík, Ph.D., přednosta Interní a kardiologické kliniky LF OU a FN Ostrava, obrátil pozornost k fenotypům a diagnostice HFpEF. Na kazuistikách tří pacientů demonstroval tři různé příčiny HFpEF. U paní Ludmily, ročník 1944, se SS vyvinulo při emergentním hypertenzním stavu, u paní Bohuslavy, ročník 1937, vzniklo SS při nově vzniklé fibrilaci s rychlou odpovědí komor a u pana Miroslava, ročník 1948, to bylo při akutním anurickém renálním selhání. Doporučené postupy ESC pro diagnostiku a léčbu SS z roku 2021 stanovují HFpEF na základě symptomatologie, výše ejekční frakce levé komory (50 % a více) a na základě objektivní přítomnosti strukturálních a/nebo funkčních abnormalit konzistentních s přítomností diastolické dysfunkce, zvýšených plnicích tlaků levé komory a také zvýšených koncentrací natriuretických peptidů. Prof. Václavík by ale spíše doporučoval diagnostický algoritmus dle HFA‑PEFF (Pieske et al., Eur Heart J Fail. 2020). Pro kardiology je zde klíčový zejména krok 2, který spočívá ve stanovení natriuretických peptidů. Pokud je NT‑proBNP u pacientů se sinusovým rytmem vyšší než 220 pg/ml nebo BNP vyšší než 80 pg/ml (nebo v případě přítomnosti fibrilace síní NT‑proBNP vyšší než 660 pg/ml, resp. BNP vyšší než 240 pg/ml), jde o tzv. velké (major) kritérium SS. Do velkých kritérií patří i morfologické ukazatele (např. LAVI nad 34 ml/m2) nebo specifikované ukazatele funkční (viz tabulku).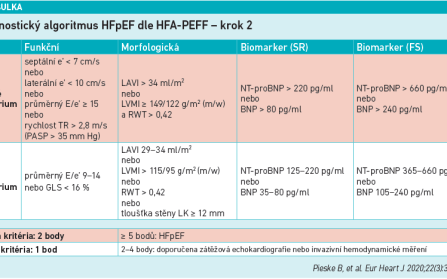 Ukazatele se skórují body, a pokud pacient dosáhne pěti bodů nebo více, je diagnóza HFpEF jistá. Pokud získá dva až čtyři body, je doporučena zátěžová echokardiografie. „Když při vyšetření pacient vyvine známky zvýšených plnicích tlaků, dostává další dva body. Pokud má navíc rychlost trikuspidální regurgitace nad 3,4 m/s, je to další bod. Pokud si ani potom stále nejsme jisti, lze ještě provést katetrizaci pravého srdce v klidu či při zátěži,“ popsal americký diagnostický postup prof. Václavík. Dodal, že čtvrtým a důležitým krokem je zjištění etiologie SS (hypertenze, chronotropní inkompetence či ischémie, kardiomyopatie apod.). „HFpEF je skutečně syndrom. Při jeho vzniku se uplatňují různé mnohočetné rizikové faktory a jejich kombinace, které vedou k abnormální struktuře či funkci myokardu. Následkem jsou různé klinické manifestace – pacient je dušný, má otoky a případně další projevy jako hypertenzi nebo fibrilaci síní. Typické jsou další komorbidity, jak už bylo řečeno – ischemická choroba srdeční, obezita, diabetes 2. typu, chronické onemocnění ledvin, mitrální nebo trikuspidální regurgitace, plicní hypertenze,“ vyjmenoval prof. Václavík. „Na rozdíl od onkologické léčby, která se staví na základě histologické a molekulárněgenetické analýzy, je léčba srdečního selhání v současné době naprosto necílená, byť dochází k jistému posunu. Víme, že existují určité klastry komorbidit, které udávají další prognózu,“ pokračoval. Objevují se totiž první práce (Uijl et al., Eur J Heart Fail. 2021), které ukazují, že pacienti s některými komorbiditami, např. hypertenzí nebo chronickým onemocněním ledvin, mají pokročilejší hypertrofii levé komory (tzv. fenotyp 2) a poměrně dobře reagují na léčbu MRA. Pak byla definována skupina pacientů, kteří mají spíše sklony k bradykardii, kongesci, elevaci GGT a celkového bilirubinu (tzv. fenotyp 3) – mají lepší přežívání na léčbě inhibitory RAAS a statiny (Sotomi et al., Heart 2023). Také ve studii TOPCAT (Cohen et al., JACC Heart Fail 2020) se podařilo identifikovat tři skupiny pacientů – jedna skupina měla normální geometrii levé komory, druhá koncentrickou remodelaci a třetí koncentrickou hypertrofii. Ukázalo se, že tyto skupiny mají různou prognózu. Třetí skupina ve studii rovněž lépe reagovala na léčbu spironolaktonem. „Snad bude do budoucna možné najít podskupiny pacientů, kteří budou dobře odpovídat na určité skupiny léků. Společným jmenovatelem všech fenotypů se ovšem zdají být inhibitory SGLT‑2, které mají na rozdíl od jiných používaných léků důkazy,“ uzavřel své sdělení prof. Václavík.
Ukazatele se skórují body, a pokud pacient dosáhne pěti bodů nebo více, je diagnóza HFpEF jistá. Pokud získá dva až čtyři body, je doporučena zátěžová echokardiografie. „Když při vyšetření pacient vyvine známky zvýšených plnicích tlaků, dostává další dva body. Pokud má navíc rychlost trikuspidální regurgitace nad 3,4 m/s, je to další bod. Pokud si ani potom stále nejsme jisti, lze ještě provést katetrizaci pravého srdce v klidu či při zátěži,“ popsal americký diagnostický postup prof. Václavík. Dodal, že čtvrtým a důležitým krokem je zjištění etiologie SS (hypertenze, chronotropní inkompetence či ischémie, kardiomyopatie apod.). „HFpEF je skutečně syndrom. Při jeho vzniku se uplatňují různé mnohočetné rizikové faktory a jejich kombinace, které vedou k abnormální struktuře či funkci myokardu. Následkem jsou různé klinické manifestace – pacient je dušný, má otoky a případně další projevy jako hypertenzi nebo fibrilaci síní. Typické jsou další komorbidity, jak už bylo řečeno – ischemická choroba srdeční, obezita, diabetes 2. typu, chronické onemocnění ledvin, mitrální nebo trikuspidální regurgitace, plicní hypertenze,“ vyjmenoval prof. Václavík. „Na rozdíl od onkologické léčby, která se staví na základě histologické a molekulárněgenetické analýzy, je léčba srdečního selhání v současné době naprosto necílená, byť dochází k jistému posunu. Víme, že existují určité klastry komorbidit, které udávají další prognózu,“ pokračoval. Objevují se totiž první práce (Uijl et al., Eur J Heart Fail. 2021), které ukazují, že pacienti s některými komorbiditami, např. hypertenzí nebo chronickým onemocněním ledvin, mají pokročilejší hypertrofii levé komory (tzv. fenotyp 2) a poměrně dobře reagují na léčbu MRA. Pak byla definována skupina pacientů, kteří mají spíše sklony k bradykardii, kongesci, elevaci GGT a celkového bilirubinu (tzv. fenotyp 3) – mají lepší přežívání na léčbě inhibitory RAAS a statiny (Sotomi et al., Heart 2023). Také ve studii TOPCAT (Cohen et al., JACC Heart Fail 2020) se podařilo identifikovat tři skupiny pacientů – jedna skupina měla normální geometrii levé komory, druhá koncentrickou remodelaci a třetí koncentrickou hypertrofii. Ukázalo se, že tyto skupiny mají různou prognózu. Třetí skupina ve studii rovněž lépe reagovala na léčbu spironolaktonem. „Snad bude do budoucna možné najít podskupiny pacientů, kteří budou dobře odpovídat na určité skupiny léků. Společným jmenovatelem všech fenotypů se ovšem zdají být inhibitory SGLT‑2, které mají na rozdíl od jiných používaných léků důkazy,“ uzavřel své sdělení prof. Václavík.
Doporučení pro diagnostiku a léčbu srdečního selhání z roku 2023 – co je nového?
Popsat novinky, které přinesla loňská aktualizace evropských doporučených postupů (ESC/HFA) 2021, měl za úkol prof. MUDr. Filip Málek, Ph.D., z Ambulance srdečního selhání a hypertenze Nemocnice Na Homolce. Update (Mc Donagh et al., Eur Heart J. 2023) se zabýval těmito okruhy: klasifikace srdečního selhání podle EF levé komory, chronické srdeční selhání, akutní srdeční selhání, komorbidity a prevence srdečního selhání. Aktualizace byla důsledkem řady nových studií, které byly publikovány mezi roky 2020 až 2023, zejména EMPEROR‑Preserved (NEJM 2021), DELIVER (NEJM 2022), STRONG‑HF (Lancet 2022), DAPA‑CKD (NEJM 2020), EMPA‑KIDNEY (NEJM 2023), FIDELIO‑DKD (NEJM 2020), FIGARO‑DKD (NEJM 2021), IRONMAN (Lancet 2023) a AFFIRM‑AHF (Lancet 2020).
Jak konstatoval prof. Málek, beze změny zůstává klasifikace SS dle EF do tří skupin. Nezměnila se ani léčba HFrEF, kdy základními pilíři jsou inhibitory ACE/ARNI, betablokátory, MRA a inhibitory SGLT‑2. Východiskem je v tomto případě klinická studie EMPEROR‑Reduced (Packer et al., NEJM 2020), která potvrdila signifikantní efekt empagliflozinu na snížení rizika úmrtí z KV příčin a hospitalizací pro SS. Pokud jde o léčbu SS s EF > 40 %, do roku 2021 žádná léčba neovlivnila morbiditu a mortalitu těchto pacientů. Základními principy léčby byla diuretika k odstranění otoků a dušnosti, adekvátní léčba hypertenze a ischémie a kontrola rytmu nebo tepové frekvence u fibrilace síní. Farmakoterapie HFpEF a HFmrEF do roku 2021 zahrnovala diuretika, betablokátory, MRA, kandesartan a inhibitory ACE na ovlivnění symptomatologie a další léky, které měly jen omezené důkazy ke snížení rizika hospitalizací (nebivolol, digoxin, spironolakton, kandesartan) nebo mortality (nebivolol, inhibitory ACE, ARB, MRA). Přelomová pro tuto skupinu nemocných byla až zmíněná studie EMPEROR‑Preserved s empagliflozinem, která hodnotila výskyt primárního sledovaného výsledného parametru úmrtí z KV příčin a hospitalizace pro srdeční selhání (Anker et al., NEJM. 2021). Podařilo se prokázat snížení relativního rizika o 21 procent a absolutního rizika o 3,3 procenta. Léčba se navíc vyznačovala velmi rychlým nástupem účinku ve srovnání s placebem. Update evropských doporučení z roku 2023 proto pro léčbu pacientů s HFmrEF uvádí, že inhibitory SGLT‑2 dapagliflozin nebo empagliflozin jsou doporučeny pro léčbu pacientů s cílem snížit riziko hospitalizace pro srdeční selhání nebo úmrtí z KV příčin (síla doporučení nejvyšší, tedy IA). Dále se doporučují diuretika při retenci tekutin. Inhibitory ACE/ARNI/ARB, stejně jako MRA, mají sílu doporučení IIb.
Doporučení pro léčbu pacientů s HFpEF jsou následující: inhibitory SGLT‑2 dapagliflozin nebo empagliflozin jsou doporučeny pro léčbu pacientů s cílem snížit riziko hospitalizace pro srdeční selhání nebo úmrtí z KV příčin. Doporučení má opět sílu IA. Diuretika mají být podána při retenci tekutin (třída důkazů I) a další léčba se odvíjí podle etiologie a komorbidit (třída důkazů I). Důležitá jsou také nová doporučení pro péči před propuštěním a časně po propuštění po hospitalizaci pro SS – strategie založená na zahájení a rychlé titraci dávek léků modifikujících průběh SS a častých a pečlivých následných kontrolách v prvních šesti týdnech po propuštění z hospitalizace je doporučena s cílem zabránit opětovné hospitalizaci a úmrtí (třída důkazů IB).
U pacientů s chronickým onemocněním ledvin jsou doporučeny inhibitory SGLT‑2 s cílem snížit riziko hospitalizace pro SS a úmrtí z KV příčin (třída důkazů IA). U pacientů s diabetem 2. typu a chronickým onemocněním ledvin je doporučen finerenon s cílem snížit riziko hospitalizace pro SS (třída důkazů IA).
Doporučené postupy pro péči o pacienty se SS a deficitem železa z roku 2023 doporučují intravenózní podávání železa (ve formě karboxymaltózy nebo derisomaltózy) u pacientů s HFrEF nebo HFmrEF s cílem zlepšit příznaky a kvalitu života a snížit riziko hospitalizace pro srdeční selhání (třída důkazů IA).
„Od roku 2021 došlo k zásadnímu vývoji poznatků v oblasti léčby srdečního selhání. Inhibitory SGLT‑2 se stávají základními léky ve všech kategoriích ejekční frakce. Prevence srdečního selhání a léčba komorbidit jsou součástí komplexní péče. Intenzivní ambulantní péče o pacienty po akutním srdečním selhání je spojena se snížením rizika hospitalizace a úmrtí. Platí, že komplexní léčbu srdečního selhání je u pacientů potřeba zahájit co nejdříve, ideálně již v průběhu hospitalizace – čas je prognóza,“ shrnul prof. Málek.
Prof. Linhart v souvislosti s požadavkem odborných doporučení na intenzivní ambulantní péči o pacienty se SS konstatoval, že Česká kardiologická společnost (ČKS) bohužel nemá v ruce žádný nástroj, jak v jednotlivých regionech optimalizovat počty ambulancí pro léčbu SS. Podle prof. Ošťádala, předsedy ČKS, je zde zásadní role zdravotních pojišťoven a regulační roli by mělo sehrát ministerstvo zdravotnictví. Úkolem ČKS je podle jejího předsedy tuto naléhavou otázku opakovaně nastolovat ve veřejné diskusi. „Stávající situaci je rozhodně třeba zlepšit a dostat se s počtem ambulancí všude na akceptovatelný průměr,“ myslí si. Prof. Táborský doplnil, že důležitá je také účast členů ČKS ve výběrových řízeních v regionech. Je podle něj možné takto podpořit ambulance tam, kde chybějí nejvíce (např. na Karlovarsku, Zlínsku, Vysočině). Budování center ambulantní péče je i úkolem pro místní samosprávy, které by měly poskytovaly nějaké incentivy, jakkoli je faktem, že se v následujících letech bude narážet na obecný nedostatek kvalifikovaného lékařského personálu.
Jak oddálit vznik SS u pacientů po infarktu myokardu?
Na otázku, jak oddálit vznik SS u pacientů po akutním infarktu myokardu (AIM), odpovídal prof. MUDr. Petr Ošťádal, Ph.D., předseda ČKS a přednosta Kardiologické kliniky 2. LF UK a FN Motol. Odpověď je podle něj zřejmá – minimalizovat poškození myokardu při AIM, a to pomocí časné reperfuze, hemodynamické stabilizace pacienta, optimalizace krevního tlaku, podání betablokátorů a inhibitorů ACE a ovlivnění ischemicko‑reperfuzního poškození. „Odumírání kardiomyocytů začíná hned po vzniku ischémie, ale my víme, že podstatná část kardiomyocytů odumře až po obnovení krevního průtoku, tedy po reperfuzi. Samotná reperfuze se tedy může na odumírání buněk srdečního svalu podílet. Nabízí se tak hypotéza, že pokud se podaří modifikovat podmínky reperfuze, můžeme snížit odumírání kardiomyocytů, a tak i zmenšit velikost infarktu,“ uvedl prof. Ošťádal. Dodal, že výzkum se tím zabývá velmi intenzivně, vznikla celá řada postupů, jak ovlivnit velikost infarktu ovlivněním podmínek reperfuze. Testována byla celá řada farmak, v současnosti ale není k dispozici žádný lék, který by prokazatelně zlepšoval ischemicko‑reperfuzní poškození. Jiný možný protektivní mechanismus představuje tzv. conditioning. Tento postup je založen na předpokladu, že pokud se při pokračující ischémii myokardu vyvolá ischémie jiné tkáně, uvolní se do krve látky, které působí protektivně na ischemický myokard při reperfuzi. Byl tak např. vyvinut přístroj k vyvolávání ischémie na horní končetině (tzv. remote ischemie) a v malé studii vedlo toto opatření ke zmenšení poškození myokardu (White et al., JACC 2015). V dalších studiích se však výsledky již nepotvrdily. Jiný postup, pomocí mechanické podpory Impella (Kapur et al., Circulation 2018), vychází pro změnu z hypotézy, že na odumírání srdečních buněk se podílí zvýšené napětí stěny levé komory – sníží‑li se toto napětí (přečerpáváním krve z levé komory před reperfuzí), dojde následně jen k menšímu poškození myokardu. Ani výsledky této studie se však nepodařilo úspěšně zopakovat. Na otázku, zda je možné modifikací podmínek při reperfuzi zmenšit velikost infarktu, a tím oddálit rozvoj SS, lze tedy říci jen to, že v současnosti dostatečná klinická evidence zatím chybí a teprve budoucí práce ukážou, zda lze reperfuzi modifikovat tak, aby vedla k ochraně myokardu.