Rizikové situace v léčbě hypertenze

Léčba arteriální hypertenze je dlouhodobá a výběr konkrétních léků, respektive jejich kombinace, má zcela zásadní vliv nejenom na účinnost, ale také na adherenci nemocných. Negativní prediktivní hodnotu má potom zejména vysoká variabilita krevního tlaku (TK) s kolísáním během dne. „Léčbu je nutné volit na míru každému nemocnému a žádoucí je volit léky s dostatečně dlouhým biologickým poločasem, tak aby byla hodnota TK co nejvyrovnanější během celého období mezi užitím tablet,“ sdělila na webináři Společnosti všeobecného lékařství ČLS JEP MUDr. Petra Vysočanová z Interní kardiologické kliniky FN Brno. Tuto část programu podpořila společnost Servier.
MUDr. Vysočanová ilustrovala své sdělení kazuistikou 50letého řidiče kamionu, který byl praktickým lékařem odeslán do specializovaného centra ke screeningu sekundární hypertenze a optimalizaci terapie. Pan Mirek trpěl hypertenzí asi deset let a měl předepsanou celou řadu léků od různých lékařů, některé duplicitně až triplicitně. Mirek ale velmi pravděpodobně neužíval žádné. Vzhledem ke své profesi neměl pravidelný režim, často zapomínal, léky nemohl v zahraničí na dálnici sehnat a byl celkově negativisticky nastaven. Jednalo se o velmi rizikového pacienta se sedavým životním stylem v nepravidelném provozu. Pan Mirek měl celou řadu komorbidit a s jen velmi omezenou adherencí. „Prvním krokem u takového pacienta je objektivizace toho, co skutečně bere. Kromě rozhovoru s nemocným se lze opřít o lékový záznam SÚKL a plazmatické koncentrace jednotlivých léků. Cenná jsou také data z kontinuálního ambulantního měření krevního tlaku s 24hodinovým průměrem. U pana Mirka bylo nutné nejprve nastolit terapeutickou důvěru a dále provést vyšetření screeningu orgánového postižení (HMOD), včetně sekundárních příčin hypertenze. Vzhledem k tomu, že žádná sekundární příčina nebyla odhalena a jednalo se o již dlouhodobě léčeného dekompenzovaného hypertonika, byla v souladu s odbornými doporučeními terapie postupně převedena na fixní trojkombinaci (konkrétně amlodipinu, perindoprilu a indapamidu). Vzhledem k objektivizované rezistentní hypertenzi byla přidána malá dávka spironolaktonu. Nemocný tak užíval dvě tablety s dostatečně dlouhým poločasem jednou denně. Kromě toho si nechal promluvit do duše, přešel jen na vnitrostátní jízdy bez směnného provozu, začal cvičit a zhubnul,“ shrnula MUDr. Vysočanová.
Léčba hypertenze je teoreticky jednoduchá
Léčba arteriální hypertenze podle platných doporučení Evropské společnosti pro hypertenzi z loňského roku (ESH 2023) [1] je podle MUDr. Vysočanové teoreticky velmi jednoduchá. Při detekci TK nad 140/90 mm Hg je namístě stanovit individualizovaný léčebný cíl a dále neprodleně zahájit terapii. V naprosté většině případů ve fixní dvojkombinaci s rychlou titrací na maximální možné dávky. Pouhé doporučení modifikace životního stylu se připouští jen u asymptomatických osob s TK pod 150/95 mm Hg a současně bez známek HMOD nebo zjevného kardiovaskulárního onemocnění. I takoví pacienti ale musejí být úzce sledováni, a pokud nedojde ke kontrole TK v následujících třech měsících, má být farmakoterapie časně zahájena. Monoterapii lze volit jen u nízce rizikových osob s TK do 150/95 mm Hg nebo s vyšším normálním tlakem a velmi vysokým kardiovaskulárním rizikem, respektive u křehkých pacientů.
I podle doporučení ESH 2023 má být léčba u většiny pacientů zahájena kombinací inhibitoru ACE (ACEI) nebo sartanu a blokátoru kalciových kanálů (BKK) nebo thiazidového/thiazide‑like diuretika, případně lze ve kterémkoli kroku zařadit betablokátor. Pokud fixní dvojkombinace ke kontrole TK nedostačuje, je namístě eskalace na fixní trojkombinaci léků ze všech tří skupin. Cílové hodnoty by se u většiny hypertoniků měly pohybovat pod 140/80 mm Hg, u mladších nemocných do 65 let je vhodné snížení systolického TK (STK) ideálně pod 130 mm Hg. Pravá rezistentní hypertenze je relativně vzácná a týká se jen pěti až deseti procent pacientů, u ostatních je na vině nízké kontroly většinou nedostatečná adherence. I proto guidelines ESH 2023 doporučují u pacientů s domnělou rezistentní hypertenzí screening non‑adherence. Skutečně rezistentní pacienty je vhodné odeslat do specializovaného centra a doplnit screening sekundární hypertenze, pokud ještě nebyl proveden. Možným krokem při léčbě rezistentní hypertenze je u pacientů s dostatečnou funkcí ledvin (eGFR > 30 ml/min/1,73 m2) přidání spironolaktonu. Je také možné volit betablokátor, alfa1‑blokátor či centrálně působící antihypertenziva.
Pozor na HMOD a sekundární hypertenzi
 Základní screening HMOD zahrnuje 12svodové EKG k detekci arytmií a známek hypertrofie levé komory, poměr albuminu a kreatininu (ACR) v moči, stanovení sérové koncentrace kreatininu, eGFR a iontogramu pro záchyt poškození ledvin. U těžké hypertenze rovněž fundoskopii pro detekci hypertenzní retinopatie. Tato vyšetření lze na základě konkrétního klinického stavu doplnit například o echokardiografii, rychlost pulsní vlny, kotníkobrachiální index, ultrazvuk karotid a ledvin, dopplerovské měření břišní aorty a renální tepny, vyšetření kognitivních funkcí nebo zobrazení mozku. U všech pacientů s hypertenzí by základní vyšetření měla být opakována alespoň jednou za dva roky, u nemocných se známkami HMOD nebo rezistentní hypertenzí častěji. Sekundární hypertenze se potom týká asi desetiny všech hypertoniků, mezi příčiny patří primární hyperaldosteronismus, obstrukční spánková apnoe, renovaskulární hypertenze a obecně onemocnění ledvin, koarktace aorty, feochromocytom nebo Cushingův syndrom. „V reálné praxi je velmi užitečným vyšetřením stanovení kalémie. I jen mírné snížení pod 3,5 mmol/l může upozornit na primární hyperaldosteronismus, který je častý a snadno léčitelný. Absence sekundární hypertenze ale nemusí znamenat, že pacient netrpí specifickým typem vysokého TK s potenciálním profitem z různých terapeutických přístupů. Například asi třetina všech hypertoniků má sůl‑senzitivní hypertenzi a tito pacienti ještě lépe než obecná populace reagují na snížení příjmu kuchyňské soli. Kromě toho jsou rozpoznávány další fenotypy a jeden přístup tak neslouží stejně dobře všem, i léčba hypertenze je stále pestřejší,“ zamyslela se MUDr. Vysočanová.
Základní screening HMOD zahrnuje 12svodové EKG k detekci arytmií a známek hypertrofie levé komory, poměr albuminu a kreatininu (ACR) v moči, stanovení sérové koncentrace kreatininu, eGFR a iontogramu pro záchyt poškození ledvin. U těžké hypertenze rovněž fundoskopii pro detekci hypertenzní retinopatie. Tato vyšetření lze na základě konkrétního klinického stavu doplnit například o echokardiografii, rychlost pulsní vlny, kotníkobrachiální index, ultrazvuk karotid a ledvin, dopplerovské měření břišní aorty a renální tepny, vyšetření kognitivních funkcí nebo zobrazení mozku. U všech pacientů s hypertenzí by základní vyšetření měla být opakována alespoň jednou za dva roky, u nemocných se známkami HMOD nebo rezistentní hypertenzí častěji. Sekundární hypertenze se potom týká asi desetiny všech hypertoniků, mezi příčiny patří primární hyperaldosteronismus, obstrukční spánková apnoe, renovaskulární hypertenze a obecně onemocnění ledvin, koarktace aorty, feochromocytom nebo Cushingův syndrom. „V reálné praxi je velmi užitečným vyšetřením stanovení kalémie. I jen mírné snížení pod 3,5 mmol/l může upozornit na primární hyperaldosteronismus, který je častý a snadno léčitelný. Absence sekundární hypertenze ale nemusí znamenat, že pacient netrpí specifickým typem vysokého TK s potenciálním profitem z různých terapeutických přístupů. Například asi třetina všech hypertoniků má sůl‑senzitivní hypertenzi a tito pacienti ještě lépe než obecná populace reagují na snížení příjmu kuchyňské soli. Kromě toho jsou rozpoznávány další fenotypy a jeden přístup tak neslouží stejně dobře všem, i léčba hypertenze je stále pestřejší,“ zamyslela se MUDr. Vysočanová.
Význam časné eskalace léčby
MUDr. Vysočanová připomněla význam časné eskalace na fixní trojkombinaci: „Trojkombinační léčba je vyhrazena pro pacienty, kteří nedosáhli dostatečné kontroly na dvojkombinační léčbě, není vhodná pro dosud naivní nemocné. Na druhou stranu, pokud dvojkombinační léčba nestačí, pak je klíčové s eskalací příliš neotálet a není důvod se trojkombinace v indikovaných případech obávat. Opět platí, že je třeba situaci hodnotit na základě konkrétního stavu. Pacient, který trpěl na dekompenzovanou hypertenzi po dlouhou řadu let, má již do jisté míry fixované postižení a nelze očekávat, že zareaguje během jednotek dnů plnou normalizací TK. Reakce u takových nemocných je spíše pozvolná, což ale není nutně špatně, naopak, prudký pokles by totiž mohl způsobit nežádoucí účinky a snížit adherenci. Trpělivost se ale vyplácí, do tří měsíců většina pacientů kontroly dosáhne. Podle multicentrické, observační, jednoramenné studie TRICOLOR [2] vedlo podávání perindoprilu, indapamidu a amlodipinu ve fixní kombinaci k dosažení cílových hodnot po prvních třech měsících léčby u více než 93 procent pacientů v běžné klinické praxi. Studie se zúčastnilo celkem 1 247 ambulantních pacientů s nekontrolovanou hypertenzí ve věku 18–79 let. Hodnot TK pod 140/90 mm Hg se povedlo dosáhnout u téměř 40 procent už po dvou týdnech léčby, tři čtvrtiny jich dosáhly po měsíci.“
Terapeutická inercie lékařů
Vedle problémů s udržením adherence komplikuje léčbu hypertenze také terapeutická inercie na straně lékaře. Mezi její projevy patří ignorování naměřených patologických hodnot a nezahájení terapie, odkládání terapie s ohledem na nízký věk pacienta nebo jeho sliby, že změní svůj životní styl, suboptimální titrace dávek či nedostatečně časná eskalace léčby. „Podstatné v tomto smyslu je, aby si své rezervy lékař aktivně uvědomil a soustředil se na z hlediska inercie rizikové situace.
Lékař, který se svou inercií aktivně pracuje, vykazuje lepší kontrolu hypertenze u svých pacientů. Suboptimální přístup bývá nejčastěji zejména vůči pacientům ve velmi mladém nebo naopak starším věku a u pacientů, jejichž hodnoty TK jsou sice patologické, ale relativně blízko normy. Přitom právě mladí pacienti jsou v konečném důsledku vysokým TK ohroženi nejvíce, protože u nich lze předpokládat, že bude kumulativně působit po nejdelší dobu,“ upozornila MUDr. Vysočanová. „Intenzivní snížení STK k cílovým hodnotám pod 120 mm Hg je oproti standardním cílům superiorní. Ve studii SPRINT [3] bylo celkem 9 361 pacientů sledováno po dobu 3,5 roku. Randomizováni byli buď k intenzivní strategii snižování STK s cílem pod 120 mm Hg, nebo ke standardní strategii s cílem STK pod 140 mm Hg. Pacienti s nižším cílem vykázali lepší výsledky. Bohužel v dlouhodobém horizontu bylo těžké tak náročné cíle udržet. V rámci studie byli pacienti i klinici motivováni, ale po jejím skončení prorazila určitá míra terapeutické inercie a snížení adherence. I přes časnou separaci křivek v průběhu studie se tyto křivky po skončení studie začaly opět zavírat. Na možnost inercie ze strany lékařů je tak třeba pomýšlet a snažit se ji omezit.“
Volbou vhodných antihypertenziv můžeme omezit variabilitu TK
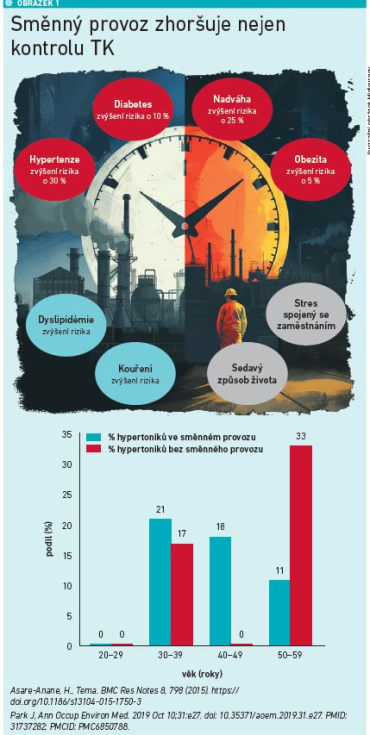
 Při výběru vhodného antihypertenziva na míru konkrétnímu nemocnému je vhodné zohlednit farmakokinetiku jednotlivých látek. Tento postup je ještě důležitější u osob s nepravidelným životním rytmem nebo u pracujících ve směnném provozu. „Noční směny jsou spojeny s negativním vlivem nejen na kardiovaskulární systém. Osoby v nočním provozu trpí na hypertenzi častěji a je u nich těžší dosáhnout její kontroly (viz obrázek 1) [4]. Proto je důležité sledovat parametry jako trough‑peak ratio – čím je nižší, tím lék vykazuje rychlejší nástup účinku a jeho časný pokles, vedoucí k vyšší variabilitě TK během dne. Naopak látky s vysokým poměrem trough‑peak mají mnohem stálejší efekt na TK, nezpůsobují přechodnou hypotenzi a udrží účinek po delší dobu. Kromě stálosti účinku je ale namístě sledovat také biologický poločas látky a volit tak, aby udržela dostatečný efekt po 24 hodin s užíváním pouze jednou denně. Zároveň nelze spoléhat na pouhý údaj o doporučeném dávkování. Mnoho léčiv má v SPC uvedeno dávkování jen jednou denně, jejich biologický poločas tomu ale neodpovídá. U osob s nepravidelným režimem je výhodné ještě o něco delší působení, které pokryje případné delší období mezi jednotlivými probuzeními, respektive lék dobře působí ještě v noci při aktivitě, kdy ostatní už dávno spí a mají fyziologicky nižší TK než přes den. Spolehlivou kontrolu TK během 24 hodin nabízejí ve svých jednotlivých skupinách především perindopril, amlodipin a indapamid,“ sdělila MUDr. Vysočanová (viz obrázek 2).
Při výběru vhodného antihypertenziva na míru konkrétnímu nemocnému je vhodné zohlednit farmakokinetiku jednotlivých látek. Tento postup je ještě důležitější u osob s nepravidelným životním rytmem nebo u pracujících ve směnném provozu. „Noční směny jsou spojeny s negativním vlivem nejen na kardiovaskulární systém. Osoby v nočním provozu trpí na hypertenzi častěji a je u nich těžší dosáhnout její kontroly (viz obrázek 1) [4]. Proto je důležité sledovat parametry jako trough‑peak ratio – čím je nižší, tím lék vykazuje rychlejší nástup účinku a jeho časný pokles, vedoucí k vyšší variabilitě TK během dne. Naopak látky s vysokým poměrem trough‑peak mají mnohem stálejší efekt na TK, nezpůsobují přechodnou hypotenzi a udrží účinek po delší dobu. Kromě stálosti účinku je ale namístě sledovat také biologický poločas látky a volit tak, aby udržela dostatečný efekt po 24 hodin s užíváním pouze jednou denně. Zároveň nelze spoléhat na pouhý údaj o doporučeném dávkování. Mnoho léčiv má v SPC uvedeno dávkování jen jednou denně, jejich biologický poločas tomu ale neodpovídá. U osob s nepravidelným režimem je výhodné ještě o něco delší působení, které pokryje případné delší období mezi jednotlivými probuzeními, respektive lék dobře působí ještě v noci při aktivitě, kdy ostatní už dávno spí a mají fyziologicky nižší TK než přes den. Spolehlivou kontrolu TK během 24 hodin nabízejí ve svých jednotlivých skupinách především perindopril, amlodipin a indapamid,“ sdělila MUDr. Vysočanová (viz obrázek 2).
Dlouhý biologický poločas perindoprilu a amlodipinu byl pozorován také v notoricky známé studii ASCOT. Základní studie ASCOT‑BPLA [5] byla uveřejněna v časopisu Lancet už v roce 2005, následovalo dlouhodobé sledování Legacy. Vlastní studie srovnávala antihypertenzní působení amlodipinu oproti atenololu, k prvnímu jmenovanému šlo při nedostatečné samostatné účinnosti přidat perindopril (na konci aktivní fáze studie u 68,4 % nemocných), k druhému bendroflumethiazid. Studie byla předčasně ukončena, protože BKK ± ACEI jasně superiorně o 11 procent oproti betablokátoru ± diuretiku snižoval celkovou mortalitu. Pacienti, kteří měli v režimu amlodipin, vykazovali statisticky signifikantně výrazněji snížený STK po celou dobu sledování. BKK ± ACEI charakterizoval také příznivější metabolický profil. „Amlodipin ± perindopril omezoval variabilitu TK během dne výrazně lépe než atenolol ± bendroflumethiazid, což by mohlo částečně objasnit výhodnější účinek této kombinace. Variabilita TK je totiž velmi silným prediktorem mortality a zvyšuje riziko závažných kardiovaskulárních příhod, především cévní mozkové příhody (CMP),“ dodala MUDr. Vysočanová.
Literatura:
- Mancia G, Kreutz R, Brunström M, et al. 2023 ESH Guidelines for the management of arterial hypertension. The Task Force for the management of arterial hypertension of the European Society of Hypertension: Endorsed by the International Society of Hypertension (ISH) and the European Renal Association (ERA). J Hypertens. 2023;41(12):1874–2071. doi: 10.1097/HJH.0000000000003480.
- Logunova N, Khomitskaya Y, Karpov Y, et al. Antihypertensive Effectiveness and Tolerability of Perindopril/Indapamide/Amlodipine Triple Single‐Pill Combination in the Treatment of Patients with Arterial Hypertension (TRICOLOR). J Hypertens. 2021 April;39:e373. doi: 10.1097/01.hjh.0000748864.41799.c9.
- SPRINT Research Group; Wright JT, Williamson JD, Whelton PK, et al. A Randomized Trial of Intensive versus Standard Blood‑Pressure Control. N Engl J Med. 2015;373(22):2103–2116. doi: 10.1056/NEJMoa1511939.
- Park S, Nam J, Lee JK, et al. Association between night work and cardiovascular diseases: analysis of the 3rd Korean working conditions survey. Ann Occup Environ Med. 2015;27:15. doi: 10.1186/s40557‑015‑0064‑1.
- Dahlöf B, Sever PS, Poulter NR, et al. Prevention of cardiovascular events with an antihypertensive regimen of amlodipine adding perindopril as required versus atenolol adding bendroflumethiazide as required, in the Anglo‑Scandinavian Cardiac Outcomes Trial‑Blood Pressure Lowering Arm (ASCOT‑BPLA): a multicentre randomised controlled trial. Lancet. 2005;366(9489):895–906. doi: 10.1016/S0140‑6736(05)67185‑1.