Kardio renální syndrom – myslí se na něj dostatečně?
Poměrně recentně byl koncept kardio‑renálního syndromu rozšířen o aspekt metabolický. Ukazuje se totiž, že metabolický profil je určující pro rozvoj postižení ledvin i kardiovaskulárních onemocnění, především srdečního selhání (SS). Pacienti v riziku rozvoje SS jsou osoby s hypertenzí, diabetem, obezitou nebo chronickým onemocněním ledvin (CKD). Právě na ně je nutné se zaměřit od samého začátku, protože časná detekce vaskulárního postižení u jedinců s rizikovými faktory a jejich intervence snižuje rozvoj manifestního SS. Dostupným markerem pro detekci časného vaskulárního postižení je stanovení albuminurie, resp. poměru albuminu a kreatininu v moči.
Problematika kardio‑renálně‑metabolického syndromu, zejména jeho časné diagnostiky, byla tématem jednoho z pravidelných vzdělávacích webinářů České kardiologické společnosti (ČKS). Prof. MUDr. Jan Krejčí, Ph.D., z I. interní kardioangiologické kliniky FN u svaté Anny v Brně připomněl, že užší koncept kardio‑renálního syndromu je nyní rozšířen do oblasti metabolické (Ndumele CE et al., Circulation 2023), protože se ukazuje, že metabolický profil je určující pro rozvoj jak postižení ledvin (CKD), tak kardiovaskulárního onemocnění. „Ve středu najdeme procesy stojící za vaskulární patologií, tedy chronický zánět, oxidační stres a metabolické odchylky typu inzulinové rezistence. Tyto procesy společně vedou k vaskulární dysfunkci, která je následně patofyziologickým podkladem rozvoje celé řady onemocnění,“ vysvětlil prof. Krejčí a dodal, že nesmírně důležitou roli hraje obezita, resp. tuková tkáň se svými endokrinními a parakrinními efekty. Je potvrzeno, že obezita má vliv na prognózu SS zdaleka největší v kontextu dalších onemocnění (např. diabetu, CKD) a rizikových faktorů (Screever EM et al., Clin Res Cardiol 2023) a za posledních 15 let dramaticky vzrostla. „Víme, že jednotlivé fenotypy srdečního selhání, zejména toho se zachovanou ejekční frakcí, vždy vycházejí z dominantních komorbidit, jako je hypertenze, obezita, diabetes 2. typu nebo chronické onemocnění ledvin,“ doplnil prof. Krejčí s odkazem na recentní práci (Anker SD et al., Eur J Heart Fail 2023). Na tyto rizikové faktory SS podle něj příhodně poukazují doporučené postupy pro léčbu srdečního selhání z roku 2022 z pera ACC/AHA. Je zřejmé, že na uvedené pacienty je nutné se zaměřit od samého začátku, neboť časná detekce vaskulárního postižení u jedinců s popsanými rizikovými faktory a jejich intervence redukuje riziko rozvoje manifestního SS.
Albuminurie, marker časného vaskulárního postižení
Albuminurie je markerem, který umožňuje detekci vaskulárního postižení. „Vyšetřením albuminurie lze chronické onemocnění ledvin a zvýšené kardiovaskulární riziko stanovit časněji než hodnocením poklesu odhadované glomerulární filtrace,“ podtrhnul prof. Krejčí. Už starší práce (Tsimikas S et al., Atherosclerosis 2015) zahrnula pacienty s albuminurií a bez albuminurie a sledovala jejich riziko KV příhody. Ukázalo se, že ve srovnání s pacienty bez předchozího infarktu myokardu (IM), kteří neměli albuminurii, měli pacienti s albuminurií více než dvojnásobně vyšší riziko kompozitního KV cílového ukazatele. Důležité je i to, že pacienti, kteří už jednou prodělali IM a neměli albuminurii, měli menší KV riziko než pacienti, kteří měli albuminurii, ale IM dosud neprodělali. „Zdá se tedy, že rizikovost albuminurie pro akutní koronární nemoc je zřetelně doložena,“ uvedl prof. Krejčí a dodal, že podobná situace panuje u SS. M. S. Khan et al. (J Am Coll Cardiol 2023) na analýze výsledků celé řady studií ukázali, že albuminurie má zásadní význam pro zvýšení rizikovosti rozvoje SS. „A od roku 2011 máme doloženo, že rizikovost pacienta roste v závislosti na závažnosti albuminurie, takový větší zlom nastává při albuminurii kolem 10 mg/g,“ řekl prof. Krejčí. Pokud má pacient proteinurii 300 mg/g, tak má riziko rozvoje srdečního selhání nebo úmrtí v jeho důsledku 3,5× vyšší než pacient s normoalbuminurií (Matsushita K et al., Am J Kidney Dis 2011).
Albuminurie jako okno do cév
Prof. MUDr. Ondřej Viklický, CSc., přednosta Kliniky nefrologie TC IKEM Praha, připomněl, že recentní práce KDIGO group (Kidney Int 2024) názorně ukazuje, že mezi poklesem glomerulární filtrace (GF) a vznikem různých srdečně‑cévních komplikací existuje závislost. „Víme také, že s nárůstem albuminurie, ale i glomerulární filtrace, lineárně stoupá riziko mortality, a to jak u diabetiků, tak u nediabetiků,“ doplnil. U osob se sníženou GF je očekávaná doba dožití výrazně zkrácena – např. pacient ve věku 55 let s normální GF má předpokládané dožití 19 let, ale pokud má GF sníženou pod 0,5 ml/min, tak mu zbývá odhadem jen sedm let (Gansevoort RT et al., Lancet 2013). V případě albuminurie je to podobné (pětapadesátiletý muž bez albuminurie může žít dalších dvacet let, ale závažná albuminurie mu může zkrátit život o deset let). Vztahy mezi albuminurií a GF a celkovou a KV mortalitou vystihují i poslední doporučení KDIGO z roku 2024. Např. ukazují, že pacienti s výbornou renální funkcí (kolem 105 ml/min/1,73 m2,) mladší 65 let, kteří ovšem mají závažnou albuminurii (stupeň A3), mají 2,4× vyšší riziko celkové mortality a až 4× vyšší riziko KV mortality. Pokud je navíc postižena GF, tak se riziko zněkolikanásobí– například diabetici se závažnou diabetickou nefropatií mohou mít riziko KV mortality vyšší až 12×. „Navzdory těmto faktům je albuminurie v klinické praxi opomíjeným markerem, a to i mezi nefrology a diabetology,“ připustil prof. Viklický a dodal, že toto vyšetření je skutečným oknem do cév, možná ještě průzračnějším než vyšetření cév oka.
Měřme u diabetiků každý rok eGFR a UACR
Stanovení albuminurie je ve skutečnosti vyšetření poměru koncentrace albuminu ke kreatininu ve vzorku ranní moči (UACR) nebo i jakékoli jednorázové moči (není třeba moč sbírat během dne). „Vyhláška o preventivních prohlídkách a dispenzární péči z roku 2016 už zastarala. Tehdy jsme si řekli, že UACR a eGFR by měly být stanoveny u všech pacientů starších 50 let, kteří mají kardiovaskulární onemocnění, hypertenzi nebo diabetes. Dnes už jsme ale dál,“ konstatoval prof. Viklický a pokračoval, že z tohoto důvodu z iniciativy České nefrologické společnosti vznikl tzv. one pager s názvem Doporučený postup pro diagnostiku a léčbu CKD u praktických lékařů. Jde o výtah současných doporučení platných také pro kardiologické pacienty, kteří ještě nejsou sledováni u kardiologů. „Máme jednoduché poselství – měřte u diabetiků každý rok eGFR a UACR. A u nediabetiků starších 50 let v riziku kardiovaskulárních onemocnění to samé jednou za dva roky. Možná je to odvážné, ale vychází to z dat,“ zdůraznil prof. Viklický. Doplnil, že třeba v Nizozemsku je tento screening prováděn již ve věku nad 30 let, což je velmi prozíravé vzhledem k tomu, že v současnosti jsou k dispozici renoprotektivní léky, které lze podávat pacientům s vaskulopatiemi včas. Studie EMPA‑Kidney (Herrington WG et al., NEJM 2023) ukázala, že pacienti s diabetickou nebo nediabetickou nefropatií léčení empagliflozinem mají signifikantně nižší riziko progrese CKD nebo KV úmrtí, a to o 28 procent. „Co to znamená pro pacienty? Pokud začnou být léčeni například při glomerulární filtraci 80–90 ml/min/1,73 m2, tak získají až 20 let do selhání ledvin. Pokud mají sníženou glomerulární filtraci a mají albuminurii, tak samozřejmě progredují rychleji, ale pokud mají glomerulární filtraci normální, tak u nich můžeme včasnou léčbou oddálit selhání ledvin bez ohledu na stupeň albuminurie,“ pokračoval prof. Viklický. Demonstruje to subanalýza studie EMPA‑Kidney (Fernandez‑Fernandez B et al., Clin Kidney J 2023), z níž vyplývá, že zejména pacienti s mírnou albuminurií mají velký profit z nasazení inhibitoru SGLT‑2.
Kardio‑renální syndrom a Národní kardiovaskulární plán
Prof. MUDr. Aleš Linhart, DrSc., přednosta II. interní kliniky 1. LF UK a VFN v Praze, představil problematiku kardio‑renálně‑metabolického syndromu očima Národního kardiovaskulárního plánu (NKP), který právě míří k finálnímu schválení českou vládou. „Data ÚZIS, která byla pro tvorbu strategií Národního kardiovaskulárního plánu zásadní, nepřekvapivě ukazují, že nemoci srdce a cév jsou stále hlavní příčinou úmrtí v ČR, byť jejich podíl na celkové mortalitě klesá v důsledku zlepšujících se výsledků léčby. Evidujeme ale konstantní nárůst kardiovaskulárních diagnóz, proto je otázkou, zda se nám podaří vůbec dohnat vyspělé západní země,“ uvedl prof. Linhart. Narážel tím na fakt, že mezi např. Francií a ČR je rozdíl věkově standardizované úmrtnosti na KV choroby propastných 24,5 procenta. Proto vznikl NKP, jehož vizí je zajistit každému obyvateli ČR možnost prevence vzniku KV onemocnění a v případě jeho rozvoje zajistit nejvyšší možnou kvalitu péče a života bez ohledu na geografickou polohu nebo stadium nemoci. Jinak řečeno, NKP pokrývá celou cestu od prevence až po specializovanou péči. Prof. Linhart se zaměřil na hypertenzi (HT) jako zásadní KV rizikový faktor. Pacientů s HT v Česku přibývá a je zřejmé, že pokud se nezačne modifikovat životní styl mladší generace, bude za 10 let v zemi o deset procent hypertoniků více. V roce 2023 bylo v ČR 2,2 mil. osob s vykázanou léčbou hypertenze, ale až 40 procent osob v populaci se potýká s vysokým krevním tlakem. Mezi lety 2013 a 2023 stoupla prevalence HT o 23 procent a podobně stoupá i prevalence SS, onemocnění chlopní a kardiomyopatií (arytmií dokonce o 38 procent). „O hypertenzi tu mluvím proto, že je spojena s velmi vysokým rizikem rozvoje srdečního selhání. Riziko této komorbidity roste už při mírné hypertenzi. Hypertonici mají navíc narůstající riziko mortality,“ podtrhnul prof. Linhart.
Asi polovina pacientů se SS má zachovanou nebo mírně sníženou ejekční frakci (HFpEF, resp. HFmrEF). Výchozí charakteristiky studií u pacientů s HFpEF a HFmrEF s glifloziny, finerenonem a sakubitril/valsartanem ukazují, že ve všech bylo 90 a více procent studijní populace současně hypertoniky a 40–45 procent diabetiky. Varující ale bylo, že polovina měla sníženou eGFR pod 60 ml/min. Screening těchto komorbidit by měl podle prof. Linharta vyústit ve správnou diagnostiku pacientů a jejich následné referování k dalším specializacím. „Národní kardiovaskulární plán si představujeme jako kaskádu možností, které poskytuje náš zdravotní systém od prevence přes časnou diagnostiku, diagnostiku komplikací pomocí jednoduchých nástrojů, jako je stanovení eGFR, UACR, NT‑proBNP, až po výstup v podobě specializované péče v praxích nefrologa, kardiologa nebo diabetologa a za jejich vzájemné spolupráce, “ shrnul prof. Linhart.
Z následné diskuse řečníků vyplynulo, že stejně tak, jako by měli kardiologové u pacientů se SS a KV onemocněním pátrat po CKD, měli by nefrologové soustředit pozornost na screening SS u svých pacientů. Podle prof. Viklického je ale určitou překážkou fakt, že k nefrologům se velká část pacientů dostává až v pokročilých stadiích onemocnění. Upozornil také na to, že marker SS, tedy koncentrace NT‑proBNP, je třeba interpretovat vzhledem ke stadiu CKD, tedy podle renálních parametrů. Je totiž známo, že např. čím nižší je GF, tím vyšší jsou hodnoty natriuretických peptidů. Klinická úvaha by tedy měla pokaždé být součástí diagnostiky. „Můžeme ale shrnout, že nefrologové by se měli více zastavovat u NT‑proBNP a kardiologové více u renálních parametrů a celý tento screening by se měl posouvat blíže primární péči, aby byli pacienti zachytáváni opravdu včas. Už jen proto, že praktičtí lékaři sledují drtivou většinu případů hypertenze, u níž je počátek všech zmiňovaných komorbidit a komplikací,“ konstatoval prof. Linhart.
Guidelines ESC pro léčbu SS z roku 2023 podtrhávají CKD a diabetes 2. typu jako diagnózy vhodné pro léčbu inhibitory RAAS, protože je potvrzeno, že se tak prezervuje funkce ledvin a snižuje riziko rozvoje albuminurie a těžšího selhání ledvin. Prevence SS u osob s diabetem a CKD dle těchto doporučení zahrnuje glifloziny pro snížení rizika hospitalizace pro SS nebo úmrtí z KV příčin (třída doporučení I, úroveň důkazů A). Tyto léky by přitom lékaři neměli používat jen u osob s rozvinutým SS, ale i u osob s diabetem a CKD, které jsou v riziku rozvoje SS, neboť tato terapie zamezí rozvoji manifestního SS (ovlivnění rizika u pacientů s CKD bez diabetu nedosáhlo statistické významnosti, proto jsou v doporučeních podmínky specifikovány na koincidenci CKD a diabetu 2. typu).
Důležité je zmínit i úhradové podmínky empagliflozinu – v indikacích diabetes 2. typu, SS a CKD jej může předepisovat diabetolog a endokrinolog, kardiolog a internista (nefrolog pak v indikaci CKD). U pacientů s CKD bez diabetu do GF 45 ml/min není třeba sledovat UACR, nad tuto hodnotu pak ano. U pacientů s CKD i diabetem je hranice eGFR 75 ml/min.
O čem nevíme, to neléčíme
MUDr. Jiří Veselý z EDUMED s. r. o. se zaměřil na otázku, do jaké míry se v klinické praxi daří využívat prognostickou léčbu u pacientů se SS a CKD. „Mnohdy jsou bariéry v léčbě mnohem jednodušší, než je např. finanční nákladnost léčby – o čem nevím, to neléčím. Pokud tedy nevíme, zda má pacient srdeční selhání se zachovanou ejekční frakcí nebo CKD, těžko ho můžeme léčit,“ vystihl situaci MUDr. Veselý. Za 16 let by přitom podle predikcí ÚZIS mělo v Česku být téměř 900 000 osob se SS (vlivem stárnutí populace, obezity, ale i lepší diagnostiky onemocnění). Podle MUDr. Veselého se diagnóza SS nestaví až tak těžce, NT‑proBNP je základní a snadný marker, který je dobře dostupný (12× za rok toto vyšetření hradí zdravotní pojišťovna), navíc jsou dnes již dostupné metody POCT hrazené klíčovým odbornostem včetně diabetologů. V řádu minut je pak možné reagovat na výsledky vyšetření úpravou medikace. Klíčovým předpokladem je podle MUDr. Veselého pozornost k problematice a snaha provádět screening.
Americká studie ADD‑CKD (Satzech LA, PlosOne 2014) zahrnula 9 000 pacientů z 500 praxí praktických lékařů nebo diabetologů. V rámci studie bylo u těchto pacientů provedeno jednorázové vyšetření renálních funkcí (eGFR a UACR). Celkem 5 000 pacientů z celkového počtu 9 000 mělo CKD. Investigátoři se následně podívali do dokumentace – jen asi 12 procent těchto pacientů mělo diagnózu CKD uvedenu ve své dokumentaci, 88 procent nikoli. „Nejhůře na tom byli pacienti s počátečními a lehčími stadii CKD. Měli bychom tedy kromě kardiologických diagnóz a diabetu 2. typu sledovat i ledviny a snažit se určit příčinu poškození jejich funkce. Měli bychom také do dokumentace důsledně zapsat výši eGFR a UACR,“ apeloval MUDr. Veselý. Evropská realita je podle něj neméně krutá. Recentní studie (Wanner C et al., 2024) sledovala téměř 450 000 pacientů z ordinací 1 244 německých praktiků. Celkem 76 procent mělo hypertenzi, 35 procent mělo KV onemocnění, 32 procent diabetes. Během sledování 1,7 roku byl sérový kreatinin změřen u 46 procent pacientů, UACR však jen u 0,4 procenta. „Smutné bylo na této studii i to, že čím více byli pacienti rizikoví, tím méně měli tato vyšetření provedena,“ podotkl MUDr. Veselý a přispěl analýzou dat vlastní ambulance. Z 3 500 pacientů EDUMED má přibližně 800 sníženou GF a abnormální albuminurii (stadia A2 a A3) má přes 600 pacientů. Zajímavý je pak i segment těch, kteří neměli sníženou GF, ale už měli albuminurii. I těchto je v ambulanci několik stovek. „Pokud tedy nebudeme vyšetřovat také UACR, nemůžeme u pacientů postavit diagnózu CKD, a tedy je adekvátně léčit. Od toho, jaká je albuminurie, se odvíjí mimo jiné to, kolikrát ročně máme pacienta vyšetřovat. Albuminurie je jednoduchý marker, který je oknem do našich cév, ale myslíme na něj málo,“ posteskl si MUDr. Veselý. I on věnoval pozornost vysokému krevnímu tlaku. Nová doporučení ESC pro léčbu hypertenze (McEwoy JW et al., Eur Heart J 2024) nabádají k rutinnímu stanovení renálních funkcí (eGFR i UACR). Pokud by pacient měl středně závažné nebo závažné CKD (eGFR pod 60 ml/min/1,73 m2 nebo albuminurie 3 mg/mmol nebo více), je doporučeno opakovat měření sérového kreatininu, eGFR a UACR aspoň každoročně (úroveň důkazů IC). Tyto guidelines také doporučují s úrovní důkazů IA, že u pacientů s hypertenzí, CKD a eGFR > 20 ml/min/1,73 m2 by měly být podány inhibitory SGLT‑2 (tedy poměrně paušálně). Jinak guidelines opakují a petrifikují potřebu inhibice RAAS pro redukci albuminurie u pacientů s hypertenzí a albuminurií či proteinurií. Až 40 procent diabetiků nad 65 let má albuminurii, takže sem je třeba upřít hodně pozornosti.
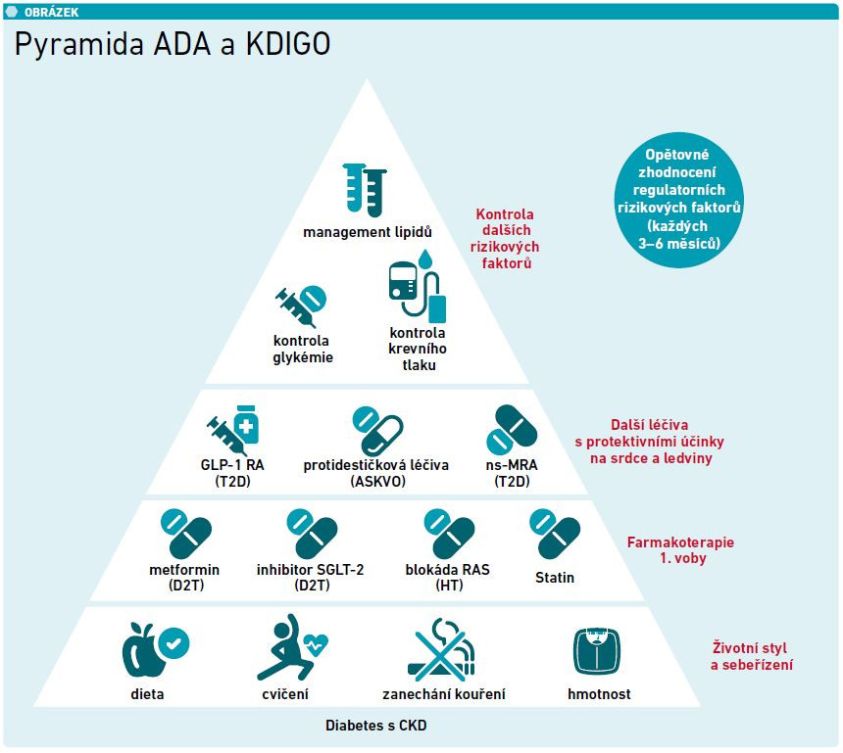
Na závěr MUDr. Veselý vyzdvihl pyramidu ADA a KDIGO (Diabetes Care 2022) (viz obrázek), která dobře ukazuje, co je třeba v managementu CKD u pacientů s diabetem dělat. Základnu pyramidy tvoří úprava životního stylu (dieta s ohledem na komorbidity, předpis pohybové aktivity, nekouření, snížení hmotnosti). Druhé patro opanovaly léky jako metformin (s ohledem na stav ledvin), inhibitory SGLT‑2, inhibitory RAAS a statiny. Ve třetím patře se nacházejí léky jako agonisté GLP‑1 (mají určitá nefroprotektivní data, ale v kombinaci s inhibitory SGLT‑2 už není jejich aditivní efekt tak výrazný, jejich místo se podle soudu MUDr. Veselého bude teprve hledat), protidestičkové léky a nesteroidní MRA (které mají data velmi slibná a mohou se stát standardem léčby). Poslední dvě patra se věnují řízení léčby dle cílových hodnot, tedy kontrole glykémie, krevního tlaku a lipidů v krvi. Má‑li pacient středně závažné nebo závažné CKD a systolický krevní tlak nad 130 mm Hg, je třeba cílit na jeho snížení (úroveň důkazů IA). „Pokud si tedy upřímně odpovíme na otázku, zda u pacientů se srdečním selháním a CKD naplno využíváme potenciál terapie pro zlepšení jejich prognózy, tak musíme konstatovat, že máme rezervy, které stojí za zamyšlení – máme totiž k dispozici spolehlivé screeningové markery a účinné terapie, které je výhodné pacientům podat co nejdříve,“ uzavřel MUDr. Veselý.