Jak dostat maximum ze systémové léčby karcinomu pankreatu
Každoroční kongres PragueONCO klade mimořádný důraz na mezioborovou diskusi o problematice solidních nádorů v celé šíři – od prevence přes diagnostiku a léčbu až po paliativní péči. Mezi přednášejícími je každoročně řada renomovaných zahraničních spíkrů, z nichž někteří se vracejí opakovaně. Mezi nimi je i prof. Gerald Prager z Lékařské univerzity ve Vídni. Ten letos vystoupil v úvodním bloku věnovaném aktuálním trendům v léčbě gastrointestinálních nádorů. Konkrétně své sdělení zaměřil na vývoj v oblasti karcinomu pankreatu.
V úvodu svého sdělení prof. Prager připomněl, že karcinom pankreatu stále představuje relativně časté maligní onemocnění s velmi špatnou prognózou. Křivky mortality a incidence jsou v tomto případě blízko sebe – vyléčených nemocných je jen velmi málo. „Pět let přežívá pouze deset procent pacientů,“ upozornil prof. Prager. Nízký podíl dlouhodobě přežívajících je dán celou řadou faktorů, mezi nimiž dominuje pozdní diagnostika a rezistence tohoto nádoru k chemoterapii i radioterapii. Jen u malé části nemocných se daří onemocnění diagnostikovat ve fázi, kdy je resekabilní. Další pacienti jsou zachyceni s hraničně resekabilním nádorem, většina však přichází již s metastatickým onemocněním. Cílem léčby je pak prodloužení přežití se zachováním kvality života a zmírnění symptomů. Mimořádně důležité je terapii přizpůsobit celkovému stavu pacienta.
 Podle prof. Pragera se i u karcinomu pankreatu zřetelně projevuje nástup personalizované medicíny, ať už jde o zohlednění mutačního statusu RAS, přítomnosti mutace BRAF, mutací BRCA1 a BRCA2, případně fúze NTRK. Na významu také nabývá mikrosatelitní nestabilita. Jednou z příčin rezistence nádorů slinivky břišní k léčbě je i přítomnost denzního nádorového stromatu. To brání distribuci léčiv do nádorové tkáně. Jeden ze směrů klinického výzkumu se proto zaměřuje na nádorové mikroprostředí a možnosti jeho ovlivnění.
Podle prof. Pragera se i u karcinomu pankreatu zřetelně projevuje nástup personalizované medicíny, ať už jde o zohlednění mutačního statusu RAS, přítomnosti mutace BRAF, mutací BRCA1 a BRCA2, případně fúze NTRK. Na významu také nabývá mikrosatelitní nestabilita. Jednou z příčin rezistence nádorů slinivky břišní k léčbě je i přítomnost denzního nádorového stromatu. To brání distribuci léčiv do nádorové tkáně. Jeden ze směrů klinického výzkumu se proto zaměřuje na nádorové mikroprostředí a možnosti jeho ovlivnění.
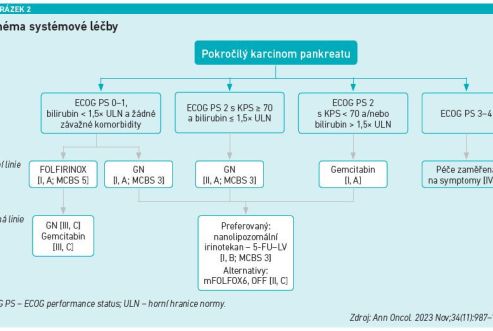 Aktuální doporučení ESMO tak už zmiňují využití cílené léčby, respektive imunoterapie u pacientů s mutací BRCA (olaparib v první linii), mikrosatelitní nestabilitou (pembrolizumab v druhé linii) a fúzí NTRK (larotrektinib v druhé linii). To se ale zatím týká jen zlomku pacientů, u všech ostatních nemocných je systémová léčba založena na chemoterapii.
Aktuální doporučení ESMO tak už zmiňují využití cílené léčby, respektive imunoterapie u pacientů s mutací BRCA (olaparib v první linii), mikrosatelitní nestabilitou (pembrolizumab v druhé linii) a fúzí NTRK (larotrektinib v druhé linii). To se ale zatím týká jen zlomku pacientů, u všech ostatních nemocných je systémová léčba založena na chemoterapii.
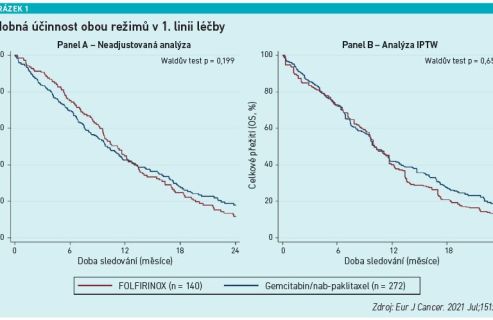
Guidelines v první linii léčby při PS 0 a 1 připouštějí jak režim FOLFIRINOX, tak gemcitabin + nab‑paklitaxel. Při PS 2 je doporučen pouze režim gemcitabin + nab‑paklitaxel a při zvýšené koncentraci bilirubinu doporučení uvádějí gemcitabin v monoterapii. Tyto režimy tvoří páteř léčby první linie. „U většiny nemocných s indikací k systémové léčbě metastatického karcinomu pankreatu budeme volit mezi režimem nab‑paklitaxel + gemcitabin a FOLFIRINOX. Nemůžeme jednoznačně říci, že jeden z těchto režimů je superiorní, a jejich využití v jednotlivých evropských zemích závisí i na úhradových podmínkách. Neexistuje prospektivní randomizovaná studie přímo porovnávající tyto dvě možnosti, recentně publikovaná data z reálné klinické praxe potvrzují, že jejich účinnost je srovnatelná (viz obrázek 1). Z hlediska toxicity je výhodnější režim nab‑paklitaxel + gemcitabin, což je důležité zvláště u starších a fragilních pacientů,“ uvedl prof. Prager s tím, že je třeba stavět celou sekvenci léčby tak, aby nemocný mohl profitovat z co nejvíce léčebných linií. I v tom je nab‑paklitaxel s gemcitabinem výhodnější, protože umožňuje v druhé linii využít režim s pegylovaným lipozomálním irinotekanem, což je i v guidelines preferovaná možnost s třídou doporučení 1B (viz obrázek 2).