Eozinofilní záněty zažívacího traktu II. část
SOUHRN
Eozinofilní záněty zažívacího traktu (eosinophilic gastrointestinal disorders, EGID) jsou onemocnění, která jsou charakterizována patologickou eozinofilní infiltrací postihující jícen, žaludek, tenké střevo nebo tračník způsobující poruchu funkce těchto orgánů a tím i odpovídající klinické příznaky. Zatímco první část tohoto článku, otištěná v minulém čísle, pojednávala o eozinofilních zánětech trávicího traktu obecně, druhá část je věnována nejčastější a nejlépe prozkoumané podjednotce – eozinofilní ezofagitidě (eosinophilic esophagitis, EoE).
Klíčová slova: eozinofilní záněty trávicího traktu • eozinofilní ezofagitida • eozinofilní gastroenteritida • eozinofilní gastritida • eozinofilní enteritida • eozinofilní kolitida
SUMMARY
Eosinophilic gastrointestinal disorders (EGID) are a group of disorders characterized by predominantly eosinophilic infiltration of the esophagus, stomach, small intestine, or colon leading to organ dysfunction and clinical symptoms. While the first part of this review, published in the last issue, discussed eosinophilic gastrointestinal disorders in general, the second part is focussed on eosinophilic esophagitis (EoE) as the most common and well recognized disorder.
Key words: eosinophilic gastrointestinal disorders • eosinophilic esophagitis • eosinophilic gastroenteritis • eosinophilic gastritis • eosinophilic enteritis • eosinophilic colitis
Koho postihuje eozinofilní ezofagitida?
Eozinofilní ezofagitida (EoE) postihuje děti i dospělé a má výraznou mužskou predilekci. Dospělí nemocní jsou ze 76 % muži, průměrný věk v době diagnózy je kolem 34 let, přičemž symptomy se manifestují průměrně 4,5 roku před diagnózou.1
Studie srovnávající nemocné s EoE a zdravé kontroly popisuje, že nemocní s EoE byli častěji nekuřáky a neměli anamnézu užívání NSAID.2 Dalšími rizikovými faktory jsou v rané vývojové fázi dítěte febrilie u matky, předčasný porod a porod sekcí, dále v dětském věku užívání antibiotik a antisekrečních léků. Zajímavým zjištěním je, že péče o domácího mazlíčka byla protektivním faktorem. Z těchto dat lze nepřímo usuzovat, že v patogenezi má určitý vliv expozice vnějším faktorům v raném dětství, a tyto asociace jsou dále zkoumány.3
Asi 75 % pacientů s EoE trpí zároveň atopickými projevy, jako jsou bronchiální astma, senná rýma nebo atopický ekzém. U pacientů s EoE je popisována sezonní variabilita potíží, což ukazuje na možnou roli inhalačních alergenů.4 V zimě, kdy je méně aeroalergenů, je diagnostikováno méně případů.5
Jak velkou roli hraje genetika?
Podle studie provedené u dětských pacientů má 5 % nemocných sourozence s EoE a 7 % jednoho z rodičů s EoE nebo se strikturou jícnu.6 U jednovaječných dvojčat vídáme EoE u obou sourozenců v 58 % případů, u dvouvaječných pak ve 36 %.7 Je vhodné poučit nemocné o možném familiárním výskytu a členy rodiny s typickými symptomy vyšetřit endoskopicky včetně biopsií. Existuje rovněž genetické testování na EoE, které může být užitečné k endofenotypizaci onemocnění.
Jaké jsou typy postižení při EoE?
Na základě zhodnocení molekulárně‑genetických markerů v kontextu endoskopických a histologických změn byly popsány tři patogeneticky odlišné endotypy EoE.8 První, mírný endotyp (EoEe1) je charakteristický mírným zánětem s minimálními endoskopickými a histologickými změnami. Druhý, zánětlivý endotyp (EoEe2) má nejvyšší expresi zánětlivých cytokinů a zahrnuje steroid‑responzivní a steroid‑refrakterní fenotyp. Třetí, fibrostenózující endotyp (EoEe3) je asociovaný s úzkým jícnem a s nejvyšším stupněm endoskopických a histologických změn. Další studie jsou potřeba k posouzení, zda endofenotypizace pacientů může pomoci v léčbě a sledování pacientů s EoE.
Jaké jsou nejčastější projevy EoE?
U dospělých jsou nejčastějšími symptomy EoE dysfagie a váznutí sousta. Studie ukazují, že EoE je diagnostikována u 15 % pacientů vyšetřovaných pro dysfagie, a dokonce až u 50 % pacientů s uvázlým soustem.9,10 Dalšími symptomy mohou být pyróza, regurgitace a bolest na hrudi, tedy symptomy vídané i u refluxní nemoci jícnu (gatroesophageal reflux disease, GERD).
Jaký je endoskopický nález?
Pacienti s EoE mají často charakteristické endoskopické známky onemocnění. U 80 % nemocných je možné nalézt příčné nebo podélné žlábky či rýhy ve sliznici, u 64 % pak slizniční prstence (obr. 1). Někdy je rýhování tak husté, že má sliznice vzhled krepového papíru (crêpe‑paper esophagus). Méně často jsou pak pozorovány bělavé papuly, striktury (zejména proximálně) či zúžení celého jícnu. Pro objektivní posouzení změn u EoE byl vyvinut endoskopický skórovací systém EREFS (Edema, Rings, Exudates, Furrows, Strictures ).11 Ačkoli je endoskopický obraz EoE poměrně specifický, někdy jsou uvedené změny velmi diskrétní a mohou být přehlédnuty, proto je doporučeno při vysokém klinickém podezření vždy provést biopsii jícnu, a to z více etáží, protože eozinofilní infiltrace nemusí být v jícnu distribuována rovnoměrně.10 Doporučuje se odebrání 2–4 bioptických vzorků z distální třetiny jícnu a dalších 2–4 bioptických vzorků ze střední nebo proximální třetiny.12
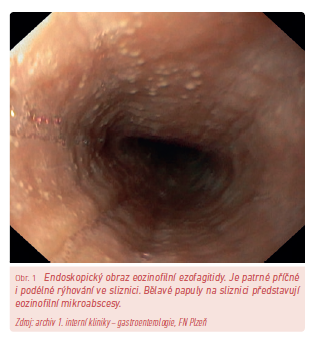
Jaký je histologický nález?
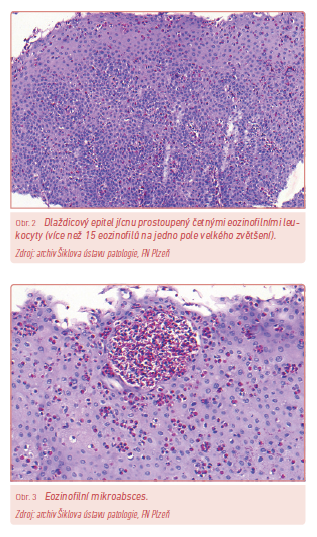
Pro diagnózu EoE se obecně vyžaduje nález minimálně 15 eozinofilů na jedno pole velkého zvětšení v dlaždicovém epitelu jícnu (obr. 2).13 Další histologické nálezy typické pro EoE představují mimo jiné eozinofilní mikroabscesy (obr. 3), degranulace eozinofilů, hyperplazie bazální membrány, subepiteliální fibróza a fibróza lamina propria.
EoE a reflux
Vztah mezi EoE a GERD je stále nejasný. Tato onemocnění mohou v jícnu koexistovat a navzájem se ovlivňovat.14 Vzhledem k podobnosti klinických symptomů a histologického nálezu může být jejich rozlišení někdy obtížné.
Provedení terapeutického testu inhibitory protonové pumpy (proton pump inhibitors, PPI) k rozlišení EoE a GERD není nápomocné. Ukázalo se, že na léčbu PPI reagují i pacienti s klinickými a histologickými známkami EoE a řadí se do kategorie tzv. PPI‑responzivní ezofageální eozinofilie.15 Rozlišit refrakterní GERD od EoE může pomoci provedení 24hodinové pH‑metrie s impedancí.
Jak se léčí?
Cílem léčby EoE je zmírnit klinické projevy a zabránit progresi onemocnění a rozvoji komplikací. Praktickým vodítkem v léčbě je krom klinického zlepšení i pokles eozinofilie v jícnu na hodnotu nižší než 15 eozinofilů na jedno pole velkého zvětšení a vymizení endoskopických známek onemocnění.
Management EoE zahrnuje farmakologickou léčbu, dietní opatření a endoskopické intervence.16 Více než polovina pacientů se symptomatickou ezofageální eozinofilií příznivě zareaguje klinicky i histologicky na léčbu PPI. Účinek PPI na EoE je patrně multifaktoriální a zahrnuje příznivý vliv na reparaci sliznice a patrně i přímý protizánětlivý efekt.17 Možný je i účinek PPI na případný koexistující GERD. Ačkoliv jejich role v léčbě EoE ještě není zcela objasněna, jsou PPI bezpečnou a účinnou úvodní léčbou.
Pokud nezareaguje na osmitýdenní kúru plnou dávkou PPI, pak je třeba zkonzultovat s nemocným další možnosti léčby. Nejčastějšími léčebnými přístupy jsou farmakologická léčba topickými kortikosteroidy nebo dietoterapie s empirickou eliminační dietou či v těžších případech s elementární dietou. Dietoterapii a postupnou reintrodukci potravin je vhodné řídit ve spolupráci s nutričními terapeuty a alergology, zvláště u pacientů s dalšími atopickými projevy.
Většina nemocných s EoE odpovídá na léčbu topickými kortikosteroidy. Nejčastěji využíváme budesonid v dávce 2 mg denně podávaný v orální viskózní suspenzi. Nejčastějším nežádoucím účinkem léčby topickými kortikosteroidy je ezofageální kandidóza.
EoE je chronické onemocnění a neléčené může vést k fibrotizaci stěny jícnu a tvorbě striktur.18 Z těchto důvodů je žádoucí nejen včas zahájit účinnou léčbu, ale rovněž zvážit podávání udržovací terapie k prevenci pokračující fibrotizace, zejména pak u nemocných s výraznou dysfagií, strikturou jícnu či s časným relapsem po iniciální léčbě.19 Nemocní s identifikovaným potravinovým spouštěčem pokračují v dietních opatřeních, u ostatních je možno pokračovat v léčbě orálním budesonidem v nejnižší účinné dávce, obvykle 1 mg denně. Absence symptomů není spolehlivým prediktorem neaktivního zánětu, proto je vhodné účinnost léčby ověřit endoskopicky a histologicky.10 Po vysazení léčby je rekurence velmi častá.
Systémová kortikoterapie není v léčbě EoE běžně používána, její klinický efekt je srovnatelný s účinkem topických přípravků a má více nežádoucích účinků.20
Endoskopická dilatace jícnových striktur uleví nemocným od dysfagie, ale nikterak nepůsobí na vlastní zánět. Tento postup je rezervován pro pacienty s fibrózními strikturami nebo prstenci, kteří neodpovídají na farmakologickou léčbu. Dilatace musí být prováděna s opatrností, protože může být komplikována hlubokou lacerací nebo perforací jícnu. Doporučuje se progrese dilatace o maximálně 3 mm při jednom sezení.21 Cílem je dosažení luminálního průměru 15–18 mm.22
Případy dysplazie nebo malignity v terénu EoE nebyly pozorovány.23
Shrnutí
- Eozinofilní záněty jsou vzácnou, ale patrně i poddiagnostikovanou skupinou onemocnění.
- U pacientů s gastrointestinálními potížemi a atopickými projevy (astma, atopický ekzém, senná rýma, potravinové alergie) je třeba vždy pomýšlet na tuto diagnózu.
- Diagnóza je stanovena na základě klinických projevů a histologického obrazu.
- Klinické projevy se odvíjejí od postižené etáže gastrointestinálního traktu a postižené vrstvy stěny a jsou velmi rozmanité. Mohou imitovat řadu běžnějších onemocnění, jako jsou refluxní nemoc jícnu, funkční dyspepsie a nespecifické střevní záněty.
- U nemocných s dysfagií a zejména s uvázlým soustem je třeba vždy pomýšlet na diagnózu eozinofilní ezofagitidy a provést mnohočetné biopsie.
- Nemocní s EGID často příznivě reagují na diety eliminující nejčastější potravinové alergeny. Jinak se léčba opírá zejména o kortikosteroidy, u EoE v podobě topického kortikosteroidu budesonidu. V případě EoE lze u velké části nemocných s efektem využít i PPI.
- EoE je chronické onemocnění a neléčené může vést k rozvoji fibrózních striktur.
Literatura
- Croese J, Fairley SK, Masson JW, et al. Clinical and endoscopic features of eosinophilic esophagitis in adults. Gastrointest Endosc 2003;58:516–522.
- Koutlas NT, Eluri S, Rusin S, et al. Impact of smoking, alcohol consumption, and NSAID use on risk for and phenotypes of eosinophilic esophagitis. Dis Esophagus 2018;31:1.
- Jensen ETKJ, Martin LJ, Rothenberg ME, Dellon ES (2018) Prenatal, intrapartum, and postnatal factors are associated with pediatric eosinophilic esophagitis. J Allergy Clin Immunol 2018;141:214–222.
- Reed CC, Iglesia EGA, Commins SP, Dellon ES. Seasonal exacerbation of eosinophilic esophagitis histologic activity in adults and children implicates role of aeroallergens. Ann Allergy Asthma Immunol 2019;122:296–301.
- Almansa C, Krishna M, Buchner AM, et al. Seasonal distribution in newly diagnosed cases of eosinophilic esophagitis in adults. Am J Gastroenterol 2009;104:828–833.
- Liacouras CA, Spergel JM, Ruchelli E, et al. Eosinophilic esophagitis: a 10‑year experience in 381 children. Clin Gastroenterol Hepatol 2005; 3:1198–1206.
- Alexander ES, Martin LJ, Collins MH, et al. Twin and family studies reveal strong environmental and weaker genetic cues explaining heritability of eosinophilic esophagitis. J Allergy Clin Immunol 2014;134:1084–1092.e1.
- Shoda T, Wen T, Aceves SS, et al. Eosinophilic oesophagitis endotype classification by molecular, clinical, and histopathological analyses: a cross‑sectional study. Lancet Gastroenterol Hepatol 2018; 3:477–488.
- Prasad GA, Talley NJ, Romero Y, et al. Prevalence and predictive factors of eosinophilic esophagitis in patients presenting with dysphagia: a prospective study. Am J Gastroenterol 2007;102:2627–2632.
- Dellon ES, Gonsalves N, Hirano I, et al. American College of Gastroenterology ACG clinical guideline: evidenced based approach to the diagnosis and management of esophageal eosinophilia and eosinophilic esophagitis (EoE). Am J Gastroenterol 2013;108:679–692; quiz 693.
- Hirano I, Moy N, Heckman MG, et al. Endoscopic assessment of the oesophageal features of eosinophilic oesophagitis: validation of a novel classification and grading system. Gut 2013;62:489–495.
- Collins MH. Histopathologic features of eosinophilic esophagitis. Gastrointest Endosc Clin N Am 2008;18:59–71.
- Furuta GT, Liacouras CA, Collins MH, et al. Eosinophilic esophagitis in children and adults: a systematic review and consensus recommendations for diagnosis and treatment. Gastroenterology 2007;133:1342–1363.
- Hirano I, Furuta GT. Approaches and Challenges to Management of Pediatric and Adult Patients With Eosinophilic Esophagitis. Gastroenterology 2020;158:840–851.
- Dellon ES, Speck O, Woodward K, et al. Markers of eosinophilic inflammation for diagnosis of eosinophilic esophagitis and proton pump inhibitor‑responsive esophageal eosinophilia: a prospective study. Clin Gastroenterol Hepatol 2014;12:2015–2022.
- Furuta GT, Katzka DA. Eosinophilic Esophagitis. N Engl J Med 2015; 373:1640–1648.
- Molina‑Infante J, Ferrando‑Lamana L, Ripoll C, et al. Esophageal eosinophilic infiltration responds to proton pump inhibition in most adults. Clin Gastroenterol Hepatol. 2011;9:110–117.
- Schoepfer AM, Safroneeva E, Bussmann C, et al. Delay in diagnosis of eosinophilic esophagitis increases risk for stricture formation in a time‑dependent manner. Gastroenterology 2013;145:1230–1236.e1–2.
- Lee JJ, Fried AJ, Hait E, et al. Topical inhaled ciclesonide for treatment of eosinophilic esophagitis. J Allergy Clin Immunol 2012;130:1011; author reply 1011.
- Arora AS, Perrault J, Smyrk TC. Topical corticosteroid treatment of dysphagia due to eosinophilic esophagitis in adults. Mayo Clin Proc 2003;78:830–835.
- Robles‑Medranda C, Villard F, le Gall C, et al. Severe dysphagia in children with eosinophilic esophagitis and esophageal stricture: an indication for balloon dilation? J Pediatr Gastroenterol Nutr 2010; 50:516–520.
- Richter JE. New questionnaire for eosinophilic esophagitis: will it measure what we want? Gastroenterology 2014; 147:1212–1213.
- Attwood SE, Smyrk TC, Demeester TR, Jones JB. Esophageal eosinophilia with dysphagia. A distinct clinicopathologic syndrome. Dig Dis Sci 1993;38:109–116.