Chronické srdeční selhání – kde jsme a kam směřujeme?
Chronické srdeční selhání v současnosti postihuje zhruba 400 000 obyvatel České republiky, ale pro rok 2040 se prevalence odhaduje zhruba na 880 000, což bude mít citelné zdravotně‑ekonomické následky pro jednotlivce i celou společnost. Dnešní medicína už ale dokáže zvrátit neblahou trajektorii progrese srdečního selhání – důležité je jejích možností využívat naplno a včas.
V rámci XXXII. výročního sjezdu České kardiologické společnosti (ČKS) proběhlo odborné sympozium společnosti Novartis, které mělo za cíl zmapovat moderní způsoby léčby srdečního selhání (SS), podívat se detailněji na problematiku náhlého úmrtí a na to, jak může v managementu chronického SS pomáhat telemedicína.
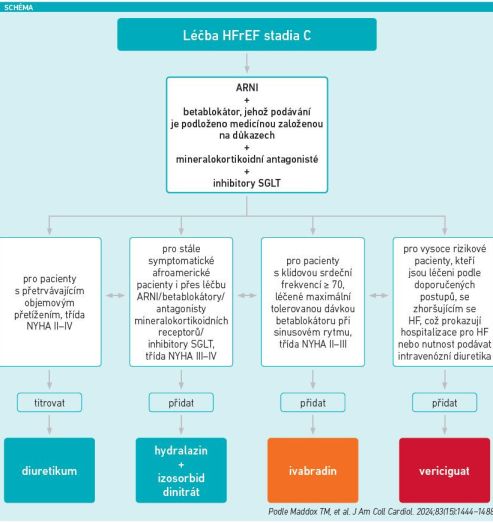 Prof. MUDr. Radek Pudil, Ph.D., z I. interní kardioangiologické kliniky FN Hradec Králové, připomněl, že v terapii SS se sníženou ejekční frakcí (HFrEF) je v popředí základní čtveřice léků, které se také uvádějí pod anglickou zkratkou GDMT (guideline‑directed medical therapy), tedy ARNI (angiotensin receptor/neprilysin inhibitor), betablokátory, antagonisté mineralokortikoidních receptorů (MRA) a inhibitory SGLT‑2 (glifloziny). Upozornil však především na dva recentní dokumenty, konsensy expertů k léčbě HFrEF a SS se zachovanou ejekční frakcí (HFpEF). „Oba dokumenty stojí za detailnější přečtení, protože podle mého názoru velmi odpovídají současnosti, jsou méně obsáhlé než americké či evropské doporučené postupy a současně jsou velmi prakticky napsané,“ doporučil prof. Pudil. Jak dokument s názvem 2024 ACC Expert Consensus Decision Pathway for Treatment of Heart Failure With Reduced Ejection Fraction: A Report of the American College of Cardiology Solution Set Oversight Committee (Maddox et al., JACC 2024), tak 2023 ACC Expert Consensus Decision Pathway on Management of Heart Failure With Preserved Ejection Fraction: A Report of the American College of Cardiology Solution Set Oversight Committee (Kittleson et al., JACC 2023) zohledňují fenotypy SS, ale promítá se tam i afroamerická problematika, která v našich podmínkách není tak frekventovaná. Pro léčbu HFrEF jsou v konsensu na prvním místě uvedeny ARNI společně s betablokátory, které mají důkazy z klinických studií (EBM), dále MRA a glifloziny. Další léčebné možnosti se odvíjejí od fenotypu SS – pokud má pacient např. retenci tekutin, jsou namístě kličková diuretika (podrobně viz schéma).
Prof. MUDr. Radek Pudil, Ph.D., z I. interní kardioangiologické kliniky FN Hradec Králové, připomněl, že v terapii SS se sníženou ejekční frakcí (HFrEF) je v popředí základní čtveřice léků, které se také uvádějí pod anglickou zkratkou GDMT (guideline‑directed medical therapy), tedy ARNI (angiotensin receptor/neprilysin inhibitor), betablokátory, antagonisté mineralokortikoidních receptorů (MRA) a inhibitory SGLT‑2 (glifloziny). Upozornil však především na dva recentní dokumenty, konsensy expertů k léčbě HFrEF a SS se zachovanou ejekční frakcí (HFpEF). „Oba dokumenty stojí za detailnější přečtení, protože podle mého názoru velmi odpovídají současnosti, jsou méně obsáhlé než americké či evropské doporučené postupy a současně jsou velmi prakticky napsané,“ doporučil prof. Pudil. Jak dokument s názvem 2024 ACC Expert Consensus Decision Pathway for Treatment of Heart Failure With Reduced Ejection Fraction: A Report of the American College of Cardiology Solution Set Oversight Committee (Maddox et al., JACC 2024), tak 2023 ACC Expert Consensus Decision Pathway on Management of Heart Failure With Preserved Ejection Fraction: A Report of the American College of Cardiology Solution Set Oversight Committee (Kittleson et al., JACC 2023) zohledňují fenotypy SS, ale promítá se tam i afroamerická problematika, která v našich podmínkách není tak frekventovaná. Pro léčbu HFrEF jsou v konsensu na prvním místě uvedeny ARNI společně s betablokátory, které mají důkazy z klinických studií (EBM), dále MRA a glifloziny. Další léčebné možnosti se odvíjejí od fenotypu SS – pokud má pacient např. retenci tekutin, jsou namístě kličková diuretika (podrobně viz schéma).
V Evropě byly loni publikovány aktualizace doporučených postupů z roku 2021, které pro třetí skupinu SS posuzovanou dle ejekční frakce, HFmrEF, doporučují diuretika, glifloziny, pak MRA a betablokátory až na místě posledním. „Neměli bychom ale na betablokátory u tohoto srdečního selhání zapomínat,“ upozornil prof. Pudil a dodal, že americká doporučení hovoří velmi podobně jako ta evropská. V případě HFpEF je však podle něho vhodné obrátit pozornost k americkým doporučením: „Nabízejí další alternativy kromě diuretik a gliflozinů, a to jít po vlastních příčinách srdečního selhání se zachovanou ejekční frakcí, kde pak mají své místo i další lékové skupiny jako MRA.“
Z pohledu ovlivňování morbidity a mortality, ale i kvality života pacientů se SS je důležité dosáhnout reverzní remodelace levé komory srdeční, kdy dochází ke zlepšování funkčních parametrů a zmenšování velikosti levé komory. „Máme k dispozici postupy, které tento fenomén navozují – jak léky, tak srdeční resynchronizační terapii a některé kardiochirurgické postupy. Farmakoterapie je ale stejně mocná v navozování reverzní remodelace levé komory nebo v prevenci náhlé srdeční smrti pacientů se srdečním selháním,“ připomněl prof. Pudil.
V druhé části svého sdělení se zaměřil na novinky poslední doby, které rozšířily poznání o povaze a léčbě SS. Za zmínku zcela jistě stojí studie STRONG‑HF (Mebazaa et al., Lancet 2022), která sledovala dva léčebné režimy u nemocných s akutním srdečním selháním, a to intenzivní přístup s titrací do maximálních dávek základních léků pro srdeční selhání a běžnou léčebnou praxi v ordinacích kardiologů. Primární cílový ukazatel zahrnoval celkovou mortalitu a rehospitalizaci pro srdeční selhání 180. den po randomizaci. Výsledkem bylo předčasné ukončení studie pro významně příznivější účinnost intenzivního přístupu, který zahrnoval léčbu betablokátory, inhibitory angiotensin konvertujícího enzymu (ACEI)/sartany nebo inhibitory ARNI, MRA (inhibitory SGLT‑2 v té době ještě nebyly schváleny pro léčbu srdečního selhání). Studie STRONG‑HF nicméně zahrnovala i pacienty se zachovanou EF LK, kteří také profitovali z včasně nasazené terapie SS. „Studie přinesla naprosto jasná data o tom, že pokud máme pacienta s akutním srdečním selháním de novo nebo s akutně dekompenzovaným chronickým srdečním selháním, vždy bychom se měli snažit dosáhnout toho, aby odcházel z nemocnice s všemi dostupnými léky, byť by to bylo i na nízké dávce. Doporučuje se zahájit terapii všemi základními skupinami léků. Vyhneme se tím takzvanému fenoménu zmařených příležitostí,“ shrnul prof. Pudil a upřesnil, že fenoménem zmařených příležitostí se rozumí situace, kdy např. ambulantní kardiologové přebírající péči o pacienta se SS mívají obavy zahájit terapii něčím jiným, novým. To pak vede k časovým prodlevám, které nejsou pro další prognózu pacienta příznivé. „Dejme si v nemocnici tu práci a připravme pečlivě propouštěcí zprávu, v níž upozorníme na potřebu titrace nebo doplnění určitého léku,“ apeloval prof. Pudil na nemocniční kardiology. Navázal informací, že kupříkladu ARNI mají účinek odbourávání natriuretických peptidů (a sekundárně je těchto peptidů produkováno méně). Na léčbě dochází k inhibici celého RAAS a ukázalo se i to, že ARNI dokáží redukovat produkci kyslíkových radikálů, tlumí zánět a apoptózu buněk. „Také u nich byla zjištěna inhibice fibrózy, která byla dosud přisuzována jen skupině MRA. Přes ovlivnění některých genových cest ARNI rovněž ovlivňují hypertrofii levé komory,“ pokračoval ve výčtu efektů ARNI prof. Pudil. Dodal, že RAAS je jednou z páteřních patofyziologických cest uplatňujících se u SS, a proto je tento systém velmi sledován a dále zkoumán. Nepatří sem jen inhibitory ACE a ARNI, ale i např. aktivátory ACE2, kam lze řadit látky uváděné pod zkratkou XNT, nebo inhibitory aldosteron syntázy. V této oblasti běží intenzivní výzkum s cílem odhalit jejich potenciál. Zajímavé jsou i některé nové směry budoucí terapie jako zárodečné (EPC) buňky nebo indukované pluripotentní kmenové (iPC) nebo mezenchymální (SPC) buňky. Předběžné výsledky podle prof. Pudila ukazují schopnost reparace tkání ve spojení s biomateriály, které jsou slibné jako náhrady tkání srdce. Ačkoli se již v některých oblastech medicíny uplatňuje léčba pomocí editace genů (CRISPR/CAS terapie), pro oblast kardiologie a léčbu SS se jedná ještě o dlouhou cestu. Ani nanočástice nejsou z výzkumu vyřazeny, testují se možnosti přímého ovlivnění cílových proteinů myokardu, ale současně se zkoumá bezpečnost nanomateriálů. Je zřejmé, že terapie SS má za sebou nejen velmi dlouhou historii, ale především pestrou současnost, která má pacientům co nabídnout.
Proč farmakologicky ovlivňovat riziko náhlé srdeční smrti?
Na tuto otázku hledala přesvědčivé odpovědi MUDr. Markéta Hegarová, Ph.D., z Kardiocentra IKEM Praha. Jednou z prvních je, že se jedná o zajištění pacientů, kteří nemají implantován kardioverter‑defibrilátor (ICD), ale i pacientů, kteří ICD mají – i oni totiž mohou zemřít náhlou smrtí, a to mechanismem elektromechanické disociace nebo rozvojem kardiogenního šoku. „Jde zejména o nemocné stabilní, málo symptomatické, např. pacienty ve funkční třídě NYHA II. Takoví jsou ve vyšším riziku náhlé srdeční smrti. Léky, které toto riziko snižují, mají celou řadu dalších benefitů, jež ústí v lepší prognózu,“ uvedla MUDr. Hegarová.
Betablokátory jsou velmi efektivní ve snižování rizika náhlé srdeční smrti, a to napříč ejekčními frakcemi a tíží symptomů – souhrnné snížení rizika náhlého úmrtí pomocí betablokátorů dedikovaných k léčbě SS je přibližně 30%. „Jedna z velkých metaanalýz ale ukazuje, že tomu tak není u pacientů se srdečním selháním a fibrilací síní. U těchto nemocných betablokátory zřejmě vůbec neovlivňují riziko kardiovaskulárního úmrtí a náhlé smrti,“ připustila MUDr. Hegarová. Dodala však, že tzv. tvrdými daty o snížení rizika náhlé smrti disponují MRA. U nich má elektrostabilizační efekt jiný mechanismus, zejména se jedná o ovlivnění myokardiální fibrózy.
Jiná je situace u inhibitorů ACE. Nikdy se nepodařilo prokázat, že by ACEI samy o sobě snižovaly riziko náhlé smrti – a to proto, že výsledky velkých mortalitních studií jsou nekonzistentní. Velká studie CONSENSUS (NEJM 1987) s enalaprilem ukázala, že nedošlo k ovlivnění náhlé smrti. Podle MUDr. Hegarové mohlo mít vliv, že pacienti ve vysoké míře užívali digoxin. Pozdější studie DIG (NEJM 1997) totiž upozornila na to, že je třeba u pacientů se SS dodržovat terapeutické koncentrace digoxinu, jinak se významně zvyšuje riziko náhlé smrti. Ve studii CONSENSUS zemřelo 11 procent pacientů náhlou smrtí, přitom měli velmi pokročilou fázi SS. Ve studii SAVE (NEJM 1992), která zkoumala efekt captoprilu na morbiditu a mortalitu pacientů s levokomorovou dysfunkcí po akutním infarktu myokardu, byl ukázán pouze trend ke snížení rizika náhlé smrti.
Pozitivní výsledky přinesla studie PARADIGM‑HF (NEJM 2014) se sakubitril/valsartanem – podařilo se prokázat, že tato léčba snižuje riziko náhlého srdečního úmrtí o 20 procent, a to u pacientů s ICD i bez něj, byť procento pacientů s ICD v této studii nebylo vysoké. Subanalýzy skupin dále ukázaly, že k ovlivnění KV mortality došlo výrazným způsobem jednak u pacientů málo symptomatických a jednak u pacientů, kteří ještě nikdy neprodělali dekompenzaci SS.
Post hoc analýza závažných nežádoucích příhod přinesla zjištění, že sakubitril/valsartan významně snížil i elektrickou nestabilitu ve smyslu snížení komorových arytmií, výbojů ICD a resuscitací pro srdeční zástavu.
Španělská studie (de Diego et al., Heart Rhytm 2018) zkoumala, co se u pacientů s HFrEF stane s komorovými arytmiemi při přechodu z ramiprilu nebo valsartanu na sakubitril/valsartan. Pacienti byli sledováni devět měsíců na konvenční léčbě, poté byli převedeni na sakubitril/valsartan. Tento postup vedl ke snížení incidence nesetrvalých komorových arytmií, komorových extrasystol, snížení výskytu fibrilace síní a zvýšení procenta biventrikulární stimulace (platí, že každé procento ovlivňuje prognózu pacientů a kvalitu jejich života). „Zajímavé je, že výskyt komorových arytmií se výrazně snížil ve vztahu k reverzní remodelaci myokardu. Ještě zajímavější ale bylo, jak výrazně došlo ke snížení míry neurohumorální aktivace u pacientů, kteří trpěli komorovými arytmiemi. Zřejmě je to velmi důležitý patofyziologický mechanismus udržení elektrické stability,“ komentovala výsledky studie MUDr. Hegarová. Dodala, že ARNI mají antifibrotický efekt, což bude zřejmě hlavní důvod, proč se jimi daří ovlivnit riziko náhlé srdeční smrti.
Lze shrnout, že k dispozici jsou silná data o významném snížení rizika náhle srdeční smrti betablokátory a blokátory mineralokortikoidních receptorů u pacientů s HFrEF. Betablokátory však neovlivňují přežívání nemocných se SS a s fibrilací síní napříč funkčními třídami a nelze předpokládat, že by u těchto nemocných snižovaly riziko náhle srdeční smrti. Data o snížení rizika náhle srdeční smrti u nemocných s HFrEF pomocí inhibitoru ACE nejsou konzistentní, nejsou k dispozici jasné důkazy. Sakubitril/valsartan však významně snižuje riziko náhle srdeční smrti u nemocných s HFrEF, a to nezávisle na implantaci ICD. Tento efekt je aditivní k léčbě betablokátory a MRA (data z velké randomizované studie). Sakubitril/valsartan také významně snižuje incidenci komorových arytmií u pacientů s HFrEF. Díky potlačení komorové ektopie zvyšuje účinnost srdeční resynchronizační léčby u pacientů s HFrEF. Příznivé účinky na riziko náhlé smrti mají také inhibitory SGLT‑2. Metaanalýzy randomizovaných studií s inhibitory SGLT‑2 ukazují na snížení rizika náhlé srdeční smrti u pacientů s HFrEF. Podle post hoc analýzy studie DAP snižuje dapagliflozin incidenci komorových arytmií a náhlé srdeční smrti u nemocných s HFrEF.
Telemedicína pomáhá v komplexním přístupu k SS
Data z NRHZS ukazují, jak dramaticky stoupá prevalence SS – jakkoli vykazování této diagnózy v klinické praxi není bez chyby, ukazuje se, že na konci roku 2023 bylo v České republice 400 000 pacientů se SS. Podle dlouhodobé predikce by pacientů se SS mělo být až 600 000 v roce 2030 a téměř 880 000 v roce 2040. Signalizuje to významný problém pro veřejné zdravotnictví i sociální systém. I digitální medicína může svým dílem přispět k řešení – základním cílem digitální medicíny u chronického SS je především snížit rehospitalizace pro dekompenzaci SS, zlepšit kvalitu života a v dlouhodobém horizontu snížit mortalitu pacientů se SS.
Jak připomněl prof. MUDr. Miloš Táborský, CSc., přednosta I. interní kardiologické kliniky FN Olomouc, telemedicína neléčí, ale pomáhá v komplexním klinickém přístupu k pacientům se SS. Má podle jeho slov v současné době dostatek důkazů u pacientů diagnostikovaných, se zavedenou terapií, vhodná je ale také u pacientů, u kterých se titruje léčba, např. ARNI, nebo u pacientů s pokročilým SS, kteří čekají na transplantaci srdce nebo mají mechanickou srdeční podporu. K dispozici jsou rovněž nové technologie, které pomáhají predikovat riziko dekompenzace SS a reagovat včas na změnu stavu pacienta.
Evropské a americké doporučené postupy pro management SS říkají, že telemedicínské služby stojí na úrovni důkazů IIB, nicméně Evropská asociace pro srdeční selhání (HFA ESC) spolu s Evropskou asociací pro srdeční rytmus (EHRA) připravují nový poziční dokument, který by měl být publikován v letošním roce a který přinese nové poznatky. Podle prof. Táborského data získaná metaanalýzou studií s telemedicínskými intervencemi ukazují přínos těchto postupů v podobě redukce mortality a rehospitalizací pro SS.
Jak vypadá situace v České republice? Mohlo by se zdát, že ČR je v oblasti telemedicíny pozadu, ale podle prof. Táborského to tak úplně není: „Máme u nás mnoho kvalitních regionálních systémů a prostředků komunikace mezi centrem a jeho pacienty. Potřebujeme však centrální platformu, která propojí jakýkoli technologický prostředek či systém napříč republikou. Taková platforma se nyní začíná v Česku soutěžit v rámci projektu NPO.“ Tato platforma by měla umožnit i sdílení dat mezi ambulantními specialisty a praktickými lékaři. Aktuálním cílem je ve třech expertních centrech vytvořit vzorové telemedicínské centrum a sdílenou aplikaci, která centra propojí v rámci bezpečného předávání dat.
Dalším důležitým posunem je EHDS, tedy systém sdílení zdravotních dat v rámci zemí EU, k jehož realizaci se ČR přihlásila v květnu 2022. Tento systém představuje možnost, jak budou moci pacienti a zdravotnická zařízení přistupovat k elektronickým zdravotním datům. Pacient má v rámci EHDS také definovánu celou řadu práv spojených s administrací svých zdravotních dat, má také např. možnost omezit třetím stranám přístup ke svým zdravotním datům.
Zásadním předpokladem úspěšného fungování eHealth je interoperabilita. Zahrnuje především pacientský souhrn, strukturovanou propouštěcí zprávu, laboratorní zprávu a již fungující nástroje, jako je eRecept a zobrazování vyšetření pomocí PACS. Současnou filosofií MZ je sjednotit regionální informační sítě do jedné centrální, která umožní nezávislou výměnu dat. Pro propouštěcí zprávy to například znamená, že budou strukturalizované, tedy bude dáno, co musejí obsahovat. „Půjde o informační bloky, které bude možné přenášet z jedné dokumentace do druhé, např. do ambulantního informačního systému,“ vysvětlil prof. Táborský a na závěr zmínil, že mezi projekty, které sice nejsou telemedicínské, ale v oblasti kardiologické léčby se povedly, patří program VZP PLUS, který byl ustanoven v roce 2022 a v roce 2023 vstoupil do širší klinické praxe. Umožnuje zjednodušeně řečeno naplňování doporučených postupů ruku v ruce s předepisováním inovativních terapií. Lékař či zdravotnické zařízení navíc získávají finanční prostředky nad rámec své dohody o úhradách. V programu VZP PLUS pro srdeční selhání se hodnotí optimalizovaná terapie SS (tj. nasazení základních čtyř skupin léků, provedení echokardiografie při pokročilém SS nebo při dekompenzaci, měření natriuretických peptidů).
Aktuálně na programu participuje 80 procent všech ambulantních kardiologů, což je podle prof. Táborského potěšující. Data VZP od téměř 8 000 pacientů ukazují, že nemocní v programu jsou v zásadě dobře léčeni – 94 procent mělo nasazenu léčbu blokující RAAS, z toho 87 procent mělo sakubitril/valsartan, pět procent inhibitor ACE a dvě procenta sartan. Celkem 96 procent dostává betablokátory, 89 procent spironolakton, 71 procent inhibitor SGLT‑2. „Překvapením je, že podle předběžných dat došlo k rehospitalizaci pro srdeční selhání u sedmi procent pacientů v programu a u 12 procent pacientů léčených standardně. To ukazuje, že správná léčba srdečního selhání podle doporučených postupů má smysl medicínský, ale bezpochyby i ekonomický. Pro rok 2025 usilujeme o to, aby bylo možné glifloziny podávat v celém spektru ejekční frakce, objeví se také vericiguat, finerenon a parenterální léčba železem,“ uzavřel prof. Táborský.