Amaurosis fugax – prchavá slepota s velkým rizikem
Amaurosis fugax je jednou z forem tranzitorní ischemické ataky. Klinickou manifestací amaurosis fugax je přechodná jednostranná ztráta zraku, která trvá několik minut. Po odeznění potíží dojde k plné obnově zrakových funkcí, a právě prchavý i bezbolestný průběh může vytvářet falešný dojem nezávažného stavu. Jeho podcenění však může vést ke vzniku ischemického iktu s trvalými nebo fatálními následky. V naší kazuistice byla opakovaná přechodná ztráta monokulárního vidění prvním příznakem 80–85% stenózy ipsilaterální arteria carotis interna. Stenóza vnitřní karotidy je nejčastější příčinou amaurosis fugax. Článek poukazuje na důležitost rychlé diagnostiky a okamžitého zahájení medikamentózní léčby a také na prospěch z časného provedení karotické endarterektomie.
Úvod
Amaurosis fugax je definována jako přechodná monokulární ztráta zraku, která trvá několik vteřin až minut, obvykle méně než 10 minut. Někdy, ale méně často, může epizoda trvat i 1–2 hodiny. Příznak je způsoben přechodnou ischemií v sítnici, cévnatce nebo zrakovém nervu. Jedná se o jednu z forem tranzitorní ischemické ataky (TIA) a jejím nejčastějším mechanismem je embolus z nestabilního aterosklerotického plátu ipsilaterální arteria carotis interna (ACI). Pacienti s amaurosis fugax by měli být akutně vyšetřeni se stejnou naléhavostí jako pacienti s akutním iktem. Vyšetření mozku pomocí výpočetní tomografie (CT) nebo magnetické rezonance (MR), stejně tak vyšetření extrakraniálních a intrakraniálních mozkových tepen jsou základními kameny úvodní diagnostiky. Doporučuje se také kardiologické vyšetření a biochemické vyšetření séra k posouzení vaskulárních rizikových faktorů.
Epidemiologie
Amaurosis fugax má roční incidenci okolo 14 případů na 100 000 obyvatel. Častěji se vyskytuje u pacientů starších 50–60 let s vaskulárními rizikovými faktory, jako je kuřáctví, arteriální hypertenze, hyperlipidemie a diabetes mellitus. Pacienti s amaurosis fugax jsou vystaveni vysokému riziku ischemické cévní mozkové příhody (iCMP) v krátkodobém i dlouhodobém horizontu. Zatímco roční riziko se dle studií odhaduje na 2–5 %, během prvních tří měsíců dosahuje riziko rozvoje iCMP 10–15 %, přičemž významnou část pacientů postihne iCMP během prvního týdne. Míra rizika také stoupá se stupněm symptomatické stenózy ACI. U symptomatické stenózy ACI > 70 % dosahuje riziko iCMP nebo smrti z vaskulárních příčin až 26 % v průběhu dvou let.
Etiopatogeneze
Příčinou amaurosis fugax je řada heterogenních onemocnění s různým stupněm závažnosti. U dospělých je nejčastější a nejzávažnější příčinou tromboembolizace z aterosklerotického plátu ipsilaterální ACI, která spolu s okluzí ACI tvoří téměř 70 % všech případů. Stump syndrom, fibrilace síní, chlopenní vady a disekce vnitřní karotidy jsou dalšími významnými příčinami, ale vyskytují se méně často. Vznik amaurosis fugax v důsledku embolizace z kardiálního zdroje je přibližně pětkrát nižší než v případě mozkového infarktu. Amaurosis fugax se může objevit i v následujících situacích: vazospasmus retinální arterie, hypoperfuze sítnice při okluzi centrální retinální tepny nebo vaskulitida.
Klinický obraz
Přechodná ztráta zraku je zpravidla náhlá, jednostranná a trvá od několika vteřin do pár minut (< 10 minut). Někdy, ale méně často, může být příhoda oboustranná nebo trvat i 1–2 hodiny. Pacienti obvykle popisují, že přes jedno oko padá clona nebo se zatahuje opona. Jiní ji líčí jako rozmazaný nebo rozpadající se obraz. Hloubka postižení může být různá, od úplné slepoty po zachování světlocitu či vnímání pohybu před postiženým okem. Po odeznění potíží dojde k plné obnově zrakových funkcí. Důležité je, že nepostižené oko má zachované normální vidění po celou dobu epizody. V době klinického vyšetření mají pacienti téměř vždy normální výsledek očního a neurologického vyšetření.
Diagnostika
Všechny případy amaurosis fugax vyžadují urgentní oftalmologické a neurologické vyšetření doplněné o krevní testy, vyšetření mozku a mozkových tepen i kardiologické vyšetření. U každého pacienta je důležité stanovit laboratorní hodnoty lipidového spektra (celkový cholesterol, triglyceridy, HDL a LDL cholesterol), glykemický profil a renální parametry. Vzhledem k široké dostupnosti a rychlosti provedení jsou standardními vstupními modalitami CT mozku a CT angiografie (CTA) mozkových tepen. Nicméně výtěžnost CT mozku je v případě TIA včetně amaurosis fugax nízká, přínos lze spatřovat především v odlišení jiné příčiny, mj. intrakraniálního krvácení či expanze. CTA poskytne vstupní vizualizaci extrakraniálních a intrakraniálních tepen, a tím i rychlou identifikaci přítomnosti okluze nebo stenózy. Hodnocení charakteru a stupně některých stenóz může být ztížené pro přítomnost výraznějších kalcifikací, proto je vhodné doplnit i duplexní sonografické vyšetření precerebrálních a cerebrálních tepen ke korelaci nálezu a získání souhrnnější informace o stavu mozkového řečiště.
Diferenciální diagnostika
Diferenciální diagnostika je poměrně široká a zahrnuje všechny ostatní příčiny způsobující přechodnou poruchu zraku. Z očních a neurologických příčin se může jednat o syndrom suchého oka, edém papily, „malý“ glaukomový záchvat, migrénu s aurou, retinální migrénu i TIA ve vertebrobazilárním povodí. Také je třeba odlišit nádor utlačující zrakový nerv nebo obrovskobuněčnou arteriitidu. Přechodnou poruchu zraku, zpravidla oboustrannou, mohou vyvolávat i běžnější situace, jako jsou hypotenze nebo kolísání glykemie u diabetika.
Léčba
 Léčba amaurosis fugax závisí na její příčině, nicméně vyšetření a léčba se musejí od počátku zaměřit na sekundární preventivní opatření ke snížení rizika iCMP v krátkodobém i dlouhodobém horizontu. Terapie má být zahájena okamžitě, resp. jakmile klinická, laboratorní a zobrazovací vyšetření mozku a mozkových tepen vyloučí jinou než ischemickou příčinu amaurosis fugax. Studie EXPRESS prokázala, že u pacientů po TIA došlo ke snížení 90denního rizika recidivy iCMP až o 80 %, pokud byla farmakologická léčba zahájena do 24 hodin. Medikamentózní léčba zahrnuje léčbu antitrombotickou (antiagregans u pacientů s nekardioembolickou TIA nebo antikoagulans s kardioembolizační TIA), statin a ovlivnění dalších modifikovatelných vaskulárních rizikových faktorů (arteriální hypertenze, diabetes mellitus či srdeční onemocnění). V indikovaných případech je prospěšné provedení karotické endarterektomie (CEA) nebo karotického stentingu.
Léčba amaurosis fugax závisí na její příčině, nicméně vyšetření a léčba se musejí od počátku zaměřit na sekundární preventivní opatření ke snížení rizika iCMP v krátkodobém i dlouhodobém horizontu. Terapie má být zahájena okamžitě, resp. jakmile klinická, laboratorní a zobrazovací vyšetření mozku a mozkových tepen vyloučí jinou než ischemickou příčinu amaurosis fugax. Studie EXPRESS prokázala, že u pacientů po TIA došlo ke snížení 90denního rizika recidivy iCMP až o 80 %, pokud byla farmakologická léčba zahájena do 24 hodin. Medikamentózní léčba zahrnuje léčbu antitrombotickou (antiagregans u pacientů s nekardioembolickou TIA nebo antikoagulans s kardioembolizační TIA), statin a ovlivnění dalších modifikovatelných vaskulárních rizikových faktorů (arteriální hypertenze, diabetes mellitus či srdeční onemocnění). V indikovaných případech je prospěšné provedení karotické endarterektomie (CEA) nebo karotického stentingu.
Kazuistika
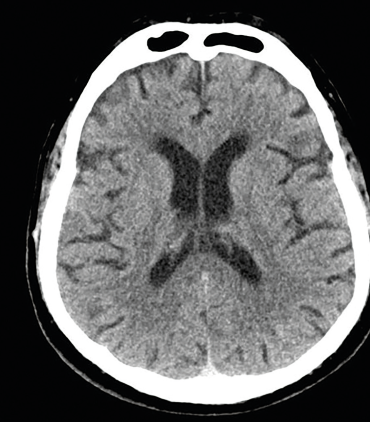
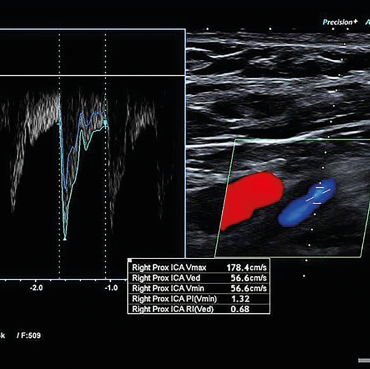
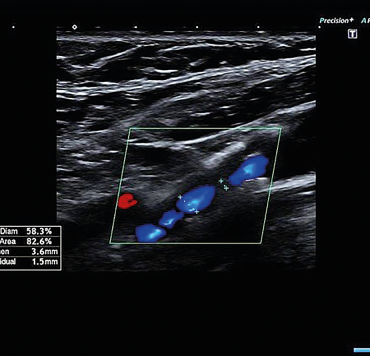
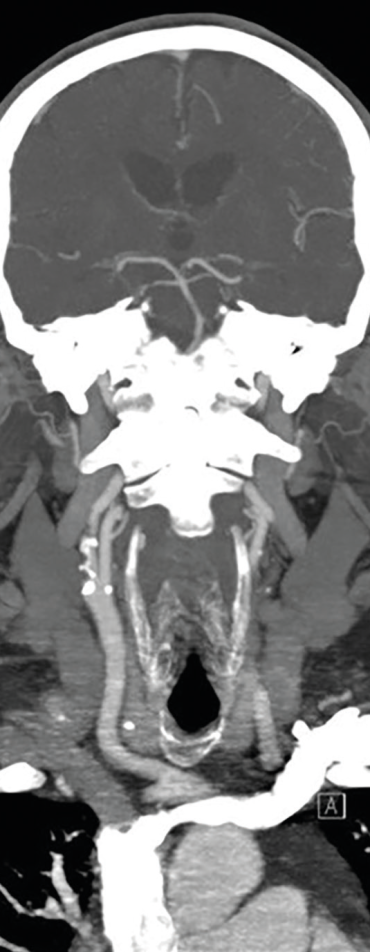 Muž, 69 let, dlouholetý kuřák, byl přijat na naše neurologické oddělení pro druhou ataku amaurosis fugax vpravo v průběhu pěti dnů. Přechodnou slepotu popisoval jako náhle vzniklý stav, při kterém měl pocit, že se mu velmi rychle vytvořila clona před pravým okem. Obě ataky prchavé monokulární amaurózy netrvaly déle než 2–3 minuty. Po druhé atace vyhledal očního lékaře, který provedl komplexní oftalmologické vyšetření včetně očního pozadí, optické koherentní tomografie a zorného pole. Nález na předním segmentu oka byl oboustranně přiměřený věku. Na očním pozadí dominovaly změny chronické hypertonické retinopatie. Zorné pole bylo v pořádku. Při přijetí na neurologické oddělení byl neurotopický nález v normě. Dle anamnézy se měl pacient léčit pro arteriální hypertenzi a hyperlipidemii, ale léky přestal užívat, protože se cítil zdráv. Při vstupním měření krevního tlaku byly zjištěny hodnoty 200/100 mm Hg. Akce srdeční byla pravidelná a vstupní elektrokardiografické vyšetření (EKG) doložilo sinusový rytmus. Fibrilace síní nebo jiná arytmie nebyly zachyceny ani při monitoraci EKG během hospitalizace na neurologické jednotce intenzivní péče (JIP). Glykemický profil byl v normě. Při vyšetření koncentrace lipidů v krvi byla zjištěna hypercholesterolemie s hodnotou LDL cholesterolu 2,94 mmol/l. Vyšetření mozku pomocí CT neprokázalo známky akutního krvácení či ischemie (obr. 1). Dle současně provedené CTA mozkových tepen byla zjištěna významná stenóza pravé ACI, nicméně hodnocení jejího stupně bylo modifikováno výraznějšími kalcifikacemi (obr. 2). Vzhledem k tomuto nálezu byla ke korelaci s CTA doplněna duplexní sonografie extrakraniálních tepen, která potvrdila 80–85% stenózu pravé ACI (obr. 3, 4). Dle transkraniální barevně kódované duplexní sonografie (TCCS) byly morfologie a hemodynamické poměry intrakraniální cirkulace v normě, nebyly zachyceny ani mikroembolické signály. V léčbě byly indikovány kyselina acetysalicylová 100 mg denně (nejprve podána nasycující dávka 300 mg) a CEA. Současně byly nasazeny atorvastatin v dávce 80 mg denně a inhibitor angiotenzin konvertujícího enzymu (ACE) v léčbě arteriální hypertenze.
Muž, 69 let, dlouholetý kuřák, byl přijat na naše neurologické oddělení pro druhou ataku amaurosis fugax vpravo v průběhu pěti dnů. Přechodnou slepotu popisoval jako náhle vzniklý stav, při kterém měl pocit, že se mu velmi rychle vytvořila clona před pravým okem. Obě ataky prchavé monokulární amaurózy netrvaly déle než 2–3 minuty. Po druhé atace vyhledal očního lékaře, který provedl komplexní oftalmologické vyšetření včetně očního pozadí, optické koherentní tomografie a zorného pole. Nález na předním segmentu oka byl oboustranně přiměřený věku. Na očním pozadí dominovaly změny chronické hypertonické retinopatie. Zorné pole bylo v pořádku. Při přijetí na neurologické oddělení byl neurotopický nález v normě. Dle anamnézy se měl pacient léčit pro arteriální hypertenzi a hyperlipidemii, ale léky přestal užívat, protože se cítil zdráv. Při vstupním měření krevního tlaku byly zjištěny hodnoty 200/100 mm Hg. Akce srdeční byla pravidelná a vstupní elektrokardiografické vyšetření (EKG) doložilo sinusový rytmus. Fibrilace síní nebo jiná arytmie nebyly zachyceny ani při monitoraci EKG během hospitalizace na neurologické jednotce intenzivní péče (JIP). Glykemický profil byl v normě. Při vyšetření koncentrace lipidů v krvi byla zjištěna hypercholesterolemie s hodnotou LDL cholesterolu 2,94 mmol/l. Vyšetření mozku pomocí CT neprokázalo známky akutního krvácení či ischemie (obr. 1). Dle současně provedené CTA mozkových tepen byla zjištěna významná stenóza pravé ACI, nicméně hodnocení jejího stupně bylo modifikováno výraznějšími kalcifikacemi (obr. 2). Vzhledem k tomuto nálezu byla ke korelaci s CTA doplněna duplexní sonografie extrakraniálních tepen, která potvrdila 80–85% stenózu pravé ACI (obr. 3, 4). Dle transkraniální barevně kódované duplexní sonografie (TCCS) byly morfologie a hemodynamické poměry intrakraniální cirkulace v normě, nebyly zachyceny ani mikroembolické signály. V léčbě byly indikovány kyselina acetysalicylová 100 mg denně (nejprve podána nasycující dávka 300 mg) a CEA. Současně byly nasazeny atorvastatin v dávce 80 mg denně a inhibitor angiotenzin konvertujícího enzymu (ACE) v léčbě arteriální hypertenze.
 Druhý den po přijetí byl pacient přeložen na Neurochirurgickou kliniku KZ, a.s. – Masarykova nemocnice v Ústí nad Labem. V regionální anestezii byla provedena endarterektomie odstupu pravé ACI. Výkon proběhl bez komplikací a pacient byl třetí pooperační den propuštěn do domácí péče. Kontrolní duplexní sonografická vyšetření provedená v naší neurosonologické laboratoři v průběhu tří, šesti a 12 měsíců po operaci prokázala normální průtok v ACI, bez známek restenózy. Při půlroční i roční klinické kontrole byl pacient bez potíží, bez recidivy amaurosis fugax či jiné TIA nebo iCMP.
Druhý den po přijetí byl pacient přeložen na Neurochirurgickou kliniku KZ, a.s. – Masarykova nemocnice v Ústí nad Labem. V regionální anestezii byla provedena endarterektomie odstupu pravé ACI. Výkon proběhl bez komplikací a pacient byl třetí pooperační den propuštěn do domácí péče. Kontrolní duplexní sonografická vyšetření provedená v naší neurosonologické laboratoři v průběhu tří, šesti a 12 měsíců po operaci prokázala normální průtok v ACI, bez známek restenózy. Při půlroční i roční klinické kontrole byl pacient bez potíží, bez recidivy amaurosis fugax či jiné TIA nebo iCMP.
Diskuse
 Neodkladně provedená klinická a zobrazovací vyšetření u pacientů s amaurosis fugax jsou zásadní pro zjištění její etiologie a nastavení sekundární prevence cerebrovaskulárních příhod. Důležité je vyšetření magistrálních mozkových tepen. Přítomnost symptomatické intrakraniální nebo extrakraniální okluze či stenózy > 50 % je podle studie CATCH nejvýznamnějším prediktorem jak pro recidivu amaurosis fugax nebo retinálního infarktu, tak především pro mozkový infarkt. Karotická endarterektomie je podle současných klinických doporučení zlatým standardem v léčbě symptomatické stenózy ACI. CEA je indikována u pacientů se 70–99% symptomatickou stenózou ACI, kterým přináší nejvýznamnější klinický přínos s absolutním snížením rizika iCMP o 16 % v průběhu následujících pěti let. Operace by měla být provedena optimálně během dvou týdnů od amaurosis fugax (2.–14. den). Čím dříve je CEA provedena, tím významnější je redukce rizika recidivy iCMP. Před provedením, v průběhu a po CEA by neměly být vysazeny ASA a statin. Věk není absolutní kontraindikací, z CEA profitují i pacienti starší 75 let, pokud nemají závažné srdeční či jiné limitující onemocnění. U pacientů se symptomatickou stenózou ACI 50–69 % může být CEA zvážena v případě, že bude provedena na pracovišti s nízkým rizikem perioperační morbidity a mortality (< 3 %), ale profit z výkonu je menší (absolutní redukce rizika o 4,6 %). Benefit CEA u pacientů s < 50% stenózou ACI nebyl prokázán.
Neodkladně provedená klinická a zobrazovací vyšetření u pacientů s amaurosis fugax jsou zásadní pro zjištění její etiologie a nastavení sekundární prevence cerebrovaskulárních příhod. Důležité je vyšetření magistrálních mozkových tepen. Přítomnost symptomatické intrakraniální nebo extrakraniální okluze či stenózy > 50 % je podle studie CATCH nejvýznamnějším prediktorem jak pro recidivu amaurosis fugax nebo retinálního infarktu, tak především pro mozkový infarkt. Karotická endarterektomie je podle současných klinických doporučení zlatým standardem v léčbě symptomatické stenózy ACI. CEA je indikována u pacientů se 70–99% symptomatickou stenózou ACI, kterým přináší nejvýznamnější klinický přínos s absolutním snížením rizika iCMP o 16 % v průběhu následujících pěti let. Operace by měla být provedena optimálně během dvou týdnů od amaurosis fugax (2.–14. den). Čím dříve je CEA provedena, tím významnější je redukce rizika recidivy iCMP. Před provedením, v průběhu a po CEA by neměly být vysazeny ASA a statin. Věk není absolutní kontraindikací, z CEA profitují i pacienti starší 75 let, pokud nemají závažné srdeční či jiné limitující onemocnění. U pacientů se symptomatickou stenózou ACI 50–69 % může být CEA zvážena v případě, že bude provedena na pracovišti s nízkým rizikem perioperační morbidity a mortality (< 3 %), ale profit z výkonu je menší (absolutní redukce rizika o 4,6 %). Benefit CEA u pacientů s < 50% stenózou ACI nebyl prokázán.
Naše kazuistika také ukazuje na význam úzké a pružné spolupráce mezi medicínskými obory, kterými v případě našeho pacienta byly oftalmologie, neurologie, radiologie a neurochirurgie.
Závěr
Amaurosis fugax je nutné hodnotit jako akutní a vysoce rizikový stav, který vyžaduje interdisciplinární spolupráci s neodkladnou diagnostikou a preventivní léčbou. Až 70 % případů je způsobeno obliterujícím onemocněním karotických tepen. Pacienti se symptomatickou stenózou ACI 70–99 % významně profitují z časně provedené CEA.
Částečně podpořeno grantem Krajské zdravotní, a.s. IGA‑KZ‑2022‑1‑5
Literatura
Bednařík J, Tomek A, Bar M, et al. Ischemická cévní mozková příhoda nebo tranzitorní ischemická ataka nekardioembolické etiologie a jejich sekundární prevence. Publikováno 2020. Národní portál klinických doporučených postupů. Registrační číslo: CZ.03.2.63/0.0/0.0/15_039/0008221.
Bonati LH, Kakkos S, Berkefeld J, et al. European Stroke Organisation guideline on endarterectomy and stenting for carotid artery stenosis. Eur Stroke J 2021;6:I–XLVII.
Coutts SB, Modi J, Patel SK, et al. Calgary Stroke Program. CT/CT angiography and MRI findings predict recurrent stroke after transient ischemic attack and minor stroke: results of the prospective CATCH study. Stroke 2012;43:1013–1017.
Ferguson GG, Eliasziw M, Barr HW, et al. The North American Symptomatic Carotid Endarterectomy Trial: surgical results in 1415 patients. Stroke 1999;30:1751–1758.
Kešnerová P. Současné možnosti využití transkraniální duplexní sonografie v cévní neurologii. Neurol praxi 2023;24:441–446.
Kvickström P, Lindblom B, Bergström G, Zetterberg M. Amaurosis fugax: risk factors and prevalence of significant carotid stenosis. Clin Ophthalmol 2016;10:2165–2170.
Makhkamova DK. Etiopathogenesis of ocular ischemic syndrome. Vestn Oftalmol 2017;133:120–124.
Pula JH, Yuen CA. Eyes and stroke: the visual aspects of cerebrovascular disease. Stroke Vasc Neurol 2017;2:210–220.
Rothwell PM, Giles MF, Chandratheva A, et al.; Early use of Existing Preventive Strategies for Stroke (EXPRESS) study. Effect of urgent treatment of transient ischaemic attack and minor stroke on early recurrent stroke (EXPRESS study): a prospective population‑based sequential comparison. Lancet 2007;370:1432–1442.
Součková D. Dnešní role duplexní sonografie u ischemické cévní mozkové příhody. Neurol praxi 2023;24:435–439.
Škoda O, Herzig R, Mikulík R, et al. Klinický standard pro diagnostiku a léčbu pacientů s ischemickou cévní mozkovou příhodou a s tranzitorní ischemickou atakou – verze 2016. Cesk Slov Neurol N 2016;79/112:351–363.
Škorňa M, Neumann J, Peška S, Mikulík R. Management tranzitorní ischemické ataky a minor stroke. Cesk Slov Neurol N 2016;112:178–187.
Štrofová H. Amaurosis fugax. Med Praxi 2016;13:72–74.